宁紫妍 王赫群
(深圳市中润医学技术研究院)
随着世界各国的疫情管控措施效果逐渐凸显,新冠疫情防控形势明显好转,其关注热度也在下降。目前各国仍未找到特效药物,虽然疫苗研发频传喜讯,但受其周期规律限制不大可能在短期上市。因此,未来在有效药物和疫苗上市前的一段时间内,各国政府可能不得不在疫情防控和恢复经济之间动态平衡。
前期新冠病毒传染之快、影响之大有目共睹,相比药物治疗在患病后干预的滞后性和无法明确的副作用,大面积接种疫苗显然是更安全、更经济的手段。国家之间,谁先掌握了疫苗,谁就掌握了经济和社会率先全面回归常态的主动权。因此,笔者一直更为关注疫苗的进展。
在疫情初期,相关疫苗公司就引起了社会广泛关注,尤其是港股上市公司康希诺生物,近期每股价格曾飙涨至285.8港币,相比最低价29.3港币,已翻8倍多,足见资本对疫苗概念的热捧态度,也说明了疫苗的重要性。除康希诺外,世界其他公司新冠疫苗项目进展如何?笔者怀着疑问整理了目前世界各地新冠疫苗研发进展情况,并对主要技术路线特点简要汇总分析。
目前全球进展情况
截至目前,新冠疫苗的最主要研发阵地在中国,而且是多种技术并举,未来也应该是新冠疫苗上市品种最多的国家。
根据世界卫生组织(WHO)的官网,截至2020年5月15日,世卫组织收集到世界各地共118个新冠疫苗候选药物研发进展信息,其中8个已进入临床试验,110个仍处于临床前评价阶段。进入临床试验的8个疫苗项目中有4个由中国研发(在5月19日国务院新闻发布会上,科技部表示全球开展临床试验的疫苗共10个,中国有5个,但未查询到相应详细信息,故本文仍沿用世卫组织统计数据)。
结合世卫组织和相关临床试验备案网站,前述8项新冠疫苗研发进展汇总如下:
表1 全球范围内已进入临床试验的疫苗项目统计
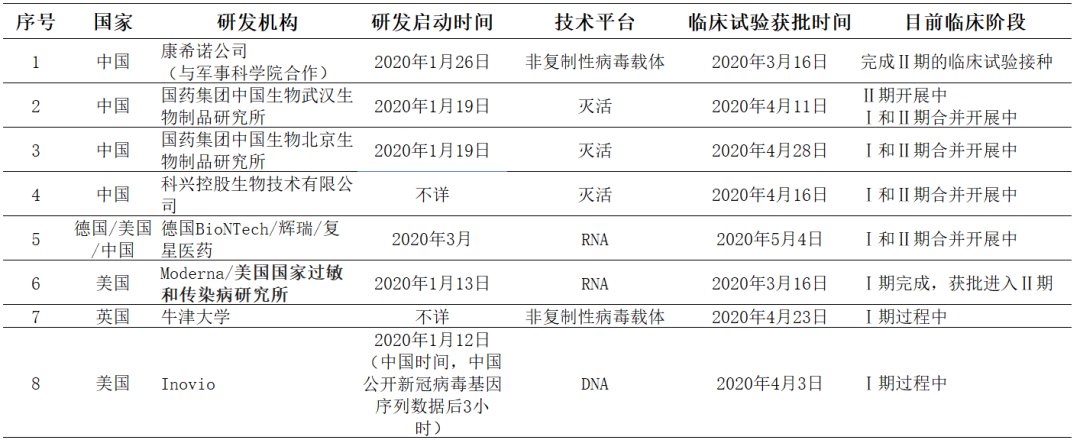
注:依据WHO公布数据和相关公司新闻报道整理。美国辉瑞和中国复星医药与德国BioNTech的合作是基于德国BioNTech的专有技术平台,美国辉瑞和中国复星医药承担的工作主要是授权许可区域内的临床试验以及上市后市场推广,主要技术应掌握在德国BioNTech手中。
根据上述统计,仅中美英德四国研发的疫苗进入临床试验,其他国家的疫苗研发还处在临床前研究阶段。中美两国跑在最前面,各有疫苗进入Ⅱ期临床试验,都预计最快在9月会有疫苗上市。个人认为,其他国家不大可能实现弯道超车,与中美同时在9月批准本国疫苗上市。
对于处于临床前研究阶段的110个疫苗项目,按照技术平台分类统计如下:
表2 全球范围内处于临床前研究阶段的新冠疫苗项目分类统计
| 技术平台 | 数量 | 占比 |
|---|---|---|
| 蛋白亚单位疫苗 | 41 | 37% |
| 复制型病毒载体疫苗 | 14 | 13% |
| RNA疫苗 | 14 | 13% |
| 非复制型病毒载体疫苗 | 13 | 12% |
| DNA疫苗 | 9 | 8% |
| 病毒样颗粒疫苗 | 7 | 6% |
| 灭活疫苗 | 5 | 4% |
| 不详 | 4 | 4% |
| 减毒活疫苗 | 3 | 3% |
| 合计 | 110 | 100% |
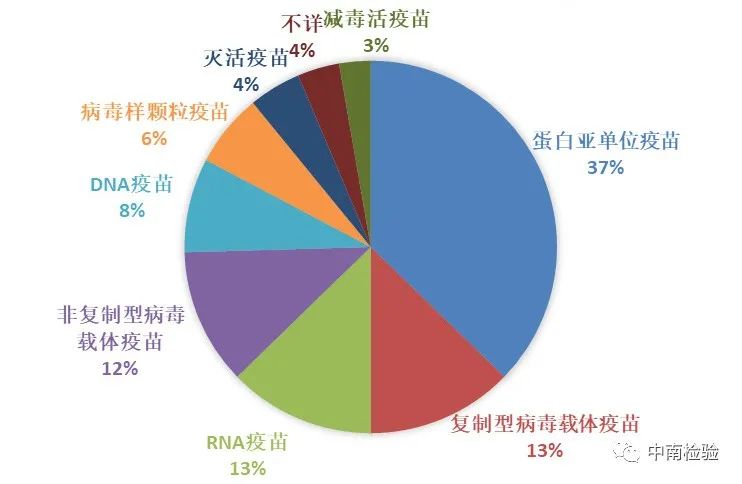
图1 处于临床前研究阶段的新冠疫苗项目技术分布图
关于疫苗技术路线
根据科技部介绍,我国新冠疫苗研发覆盖了5条技术路线,分别是:
-
灭活疫苗
-
腺病毒载体疫苗
-
基因工程重组亚单位疫苗
-
减毒流感病毒载体疫苗
-
核酸疫苗
表3 国内新冠疫苗技术路线各参数对比
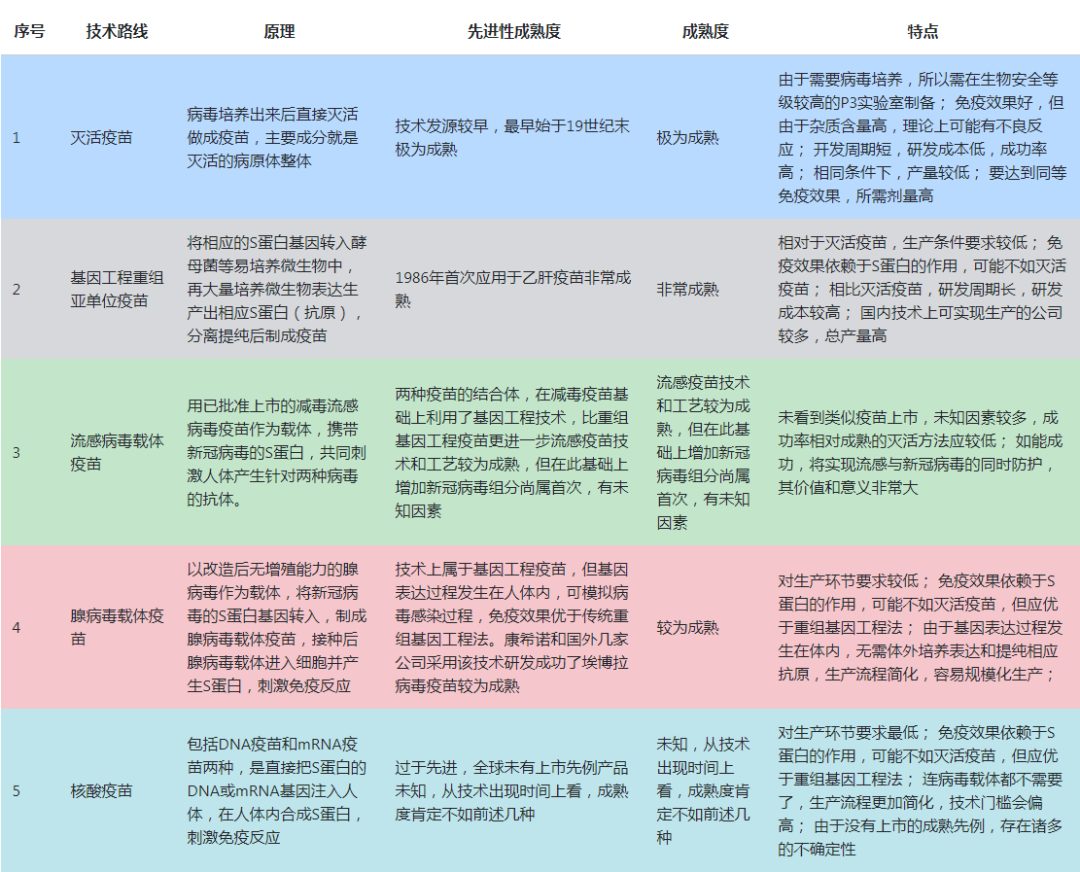
根据上述技术特点分析,目前全球新冠疫苗项目中,中国仅有灭活和腺病毒载体两种技术平台疫苗进入临床试验,而美国进入临床试验的疫苗全部为核酸技术疫苗。从结果看,中国路线偏保守,美国思路则非常激进。
灭活疫苗在技术上发源较早,发展至今工艺成熟度方面应该没有问题,但其制作原理就决定了其杂质含量相对较高,安全性上可能不及重组基因工程疫苗和腺病毒载体疫苗理想,但这种技术应用历史悠久,相信其各方面表现都会在可接受范围内。
相比其他四种基因组分疫苗技术路线,理论上灭活疫苗应具有更好的免疫效果。基因组分疫苗以S蛋白为关键免疫组分,如果未能刺激人体产生足够保护作用,那么有效性将大打折扣。根据国内研究者在《科学》杂志(《Science》)上发表的论文,灭活疫苗在动物实验中表现出保护作用,能有效抵抗新冠病毒的直接攻击。而近几天国外研究者发布的动物实验研究结果表明,接种重组腺病毒载体疫苗的动物并未得到疫苗的保护作用,参与疫苗注射的恒河猴均感染了新冠病毒。这样一来,腺病毒载体疫苗最终能否被证明具备有效性还存疑。以此类推,其他几种基因组分疫苗可能也面临这个问题。
其实腺病毒载体疫苗技术已有获批上市的成功经验,之前世界各地多个科研团队都采用该技术开发出了埃博拉疫苗。康希诺开发的埃博拉疫苗在2017年10月于国内获批上市,作为国家应急储备使用。虽然国外关于腺病毒载体疫苗的动物实验研究结果并不乐观,但最终还要看已开展的临床试验评价结果,姑且以审慎乐观的态度观察。
以乙肝疫苗为代表的重组基因工程疫苗技术也非常成熟,国内采用相关技术和工艺的生产企业较多,容易在短期内形成大规模产能,可惜的是还未进入临床试验,进展相对偏慢。但如果能在后期快速进入临床试验,也值得期待。
流感病毒载体的新冠疫苗本质上属于对已上市产品的升级改造,如能成功,临床意义最大。在未来流感爆发季,可有效降低流感和新冠疫情的叠加影响。但改造也是一种创新,创新就必然存在失败的风险,仍存在不确定性。
至于核酸疫苗,笔者并不看好。步子迈得太大,容易出问题,一项并未取得过人用疫苗商业化成功案例的技术,失败的概率还是相对较大。即便是技术先进的SpaceX,其2015年首次发射试验也是失败的。在一个如此重大疫情面前,应用新技术快速反应的初衷必然是好的,但疫苗事关大众健康甚至性命,若在短期内把一个未经时间验证的新技术产品仓促推进,再向普通大众推广,这种赶鸭子上架式的做法则应三思。好在国内研发最快的是灭活疫苗和腺病毒载体疫苗这两种相对更成熟的技术路线,足见中国管理者的智慧,而美国却押注在核酸疫苗。
对新冠疫苗下一步进展的看法
早期疫苗项目已将可能的技术路线全面覆盖,现在不大可能出现新的研发者,一方面容易造成重复投资、重复试验,势必造成资源的浪费,另一方面,后面的进入者也面临投资风险和市场压力。
如果在疫情放缓发展的今天还未进入临床试验阶段,估计后期进入疫苗市场竞争的赛道难度就更大了,毕竟临床试验资源越来越少,未进入临床的技术平台更可能作为技术储备。即便后期进入临床试验,也只能作为第二梯度进入市场,上市时间将大大晚于目前已开展临床试验的项目。
前面提到,其他几种基因组分疫苗都存在各种不确定性,仅有美国德国的核酸疫苗进入临床试验。但是美国Moderna公司迄今未对外提供过信服的实验数据,真实有效性遭到质疑,核酸疫苗能否走到最后还未知。国内核酸疫苗技术起步晚,迄今也未有进入临床试验的项目,进度上滞后于美国和德国。
全球来看,按照当前进度,年底前第一批最先批准上市的可能是中国武汉生物制品所、北京生物制品所和科兴生物公司的灭活疫苗,康希诺公司的腺病毒载体疫苗,美国Moderna公司的RNA疫苗。第二批上市的可能是牛津大学的腺病毒载体疫苗和德国BioNTech公司的RNA疫苗。第三批上市的可能是美国Inovio公司的DNA疫苗、强生公司的腺病毒载体疫苗以及赛诺菲与葛兰素史克联合开发的佐剂疫苗。
关于产能建设
疫苗的研发成功后,如能顺利通过临床试验和审批,就要面临规模化生产的问题。
根据摩根士丹利的一份分析报告,最有希望的6种新冠候选疫苗研发厂家计划2020年底前实现年产量1亿支,部分厂家在2021年年产量会达到10亿支。
国内灭活疫苗基本不存在量产的问题。中国生物申报新冠疫苗临床试验批次产量超过5万剂,量产后每批次产量超过300万剂,年产能达到1亿剂以上。2020年5月12日,国内首家人用P3生物医药生产车间项目顺利完成交付。
但笔者关注到,康希诺似乎并未在国内规划大规模生产,而是选择与加拿大合作,准备在加拿大蒙特利尔进行规模化生产。这里面可能涉及到关键的HEK293细胞系,该细胞系是生产病毒的细胞系,应该是重要的工业化规模生产载体,但却是加拿大国家研究委员会(NRC)的研究成果。康希诺在科创板的招股说明书中披露,其与NRC签订了全球非独家许可协议,可以在全球范围内使用该细胞系主细胞库及相关专利,永久有效。考虑到之前的一些风波,建议康希诺抓紧克服难题,在国内布局利用该细胞系的大规模生产。如今的跨国生产管理,很大程度上要经受国际关系波动的考验。虽然康希诺的疫苗在临床试验跑在了前面,未来在产能上可能会不及灭活疫苗。
结论
国内最终最先上市的可能是灭活疫苗,从国外动物实验结果看,腺病毒载体疫苗可能效果不佳,而且灭活疫苗产能应该比腺病毒载体疫苗产能更有保证,市场占有率应该是最高的。
目前灭活疫苗被证明是保护作用也是最好的,经过这么长时间的应用,其安全性也应该在可接受范围内。
其他技术路线的疫苗,都存在一定概率的失败风险。
中国选择的灭活疫苗和腺病毒载体疫苗这两条技术路线比较稳妥,相比之下,美国“艺高人胆大”,全押注在核酸疫苗,失败风险是蛮大的。欧洲起码还有英国牛津的腺病毒载体疫苗托底,成功几率更大些。
当然不排除美国出现技术大爆发或降低对核酸疫苗的审批标准,那么核酸疫苗成功上市,也是全人类的进步。但新技术未必适合在全世界推广,中国也有核酸疫苗的技术储备,最后能帮助全世界的,可能还要靠灭活疫苗和腺病毒载体疫苗。
疫情面前,人类终究还是命运共同体。习近平主席在第73届世界卫生大会视频会议开幕式上表示,中国新冠疫苗研发完成并投入使用后,将作为全球公共产品,为实现疫苗在发展中国家的可及性和可担负性作出中国贡献。相比一些发达国家在处置疫情不力后反而疯狂甩锅的行为,中国显然更有大国担当。期望中国的疫苗早日顺利完成临床试验,并顺利通过审批,这不仅会造福全人类,也势必会在当前国际形势下提升国家影响力。
来源:中南检验
编辑:Steven | 校对:Harris | 责编:Hillson
end
往期推荐





