

(来源:国家卫生健康委员会政务服务平台)
根据《病原微生物实验室生物安全管理条例》的规定,中华人民共和国卫生部组织制订了《人间传染的病原微生物名录》,根据全文进行汇总整理,具体如下:
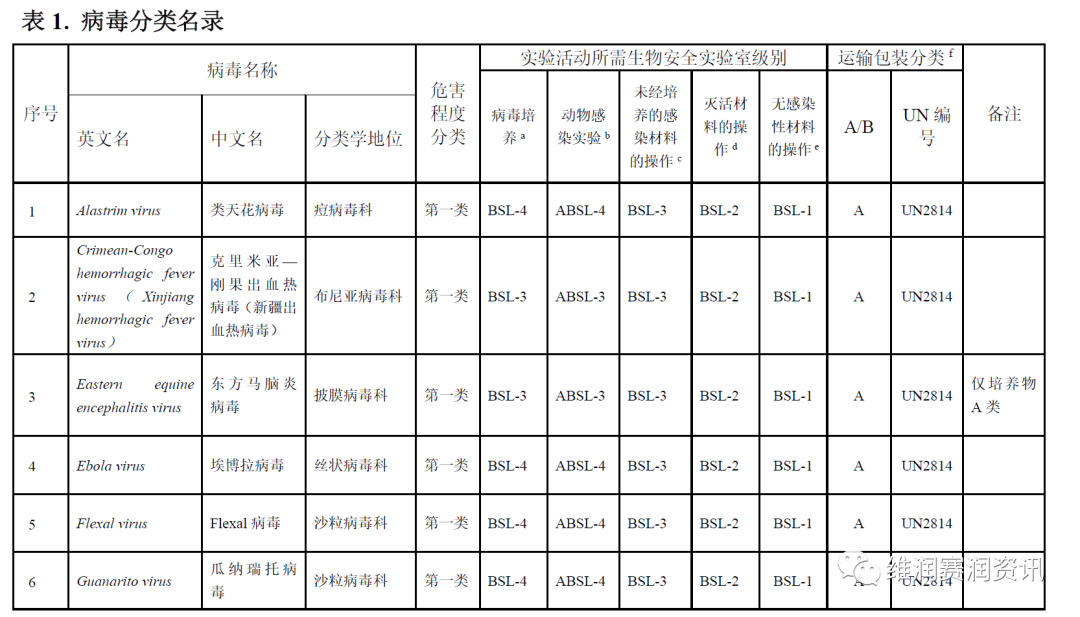
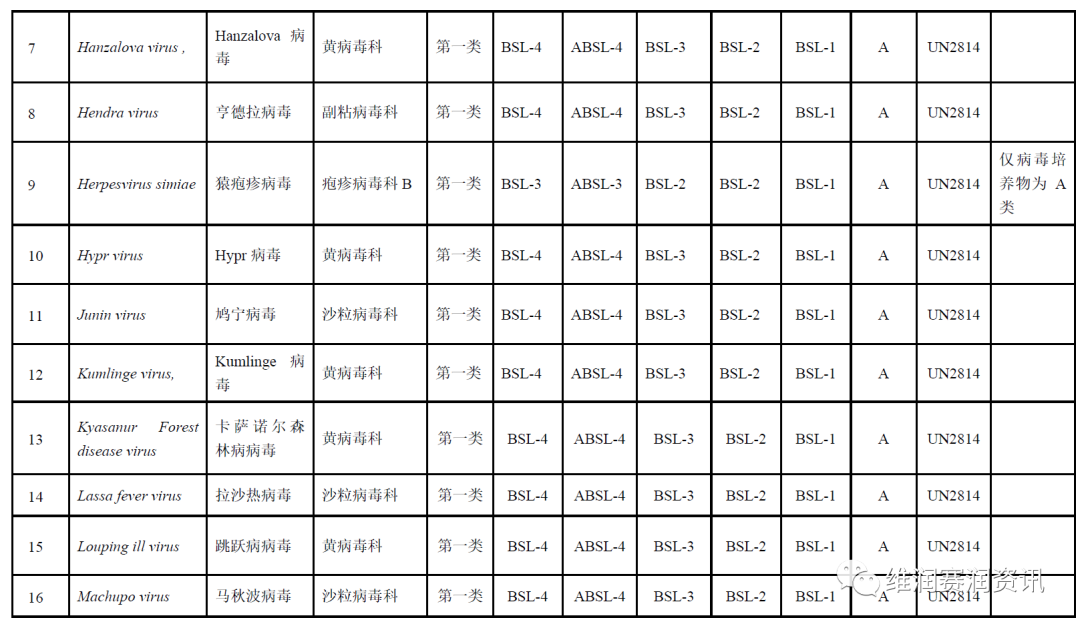
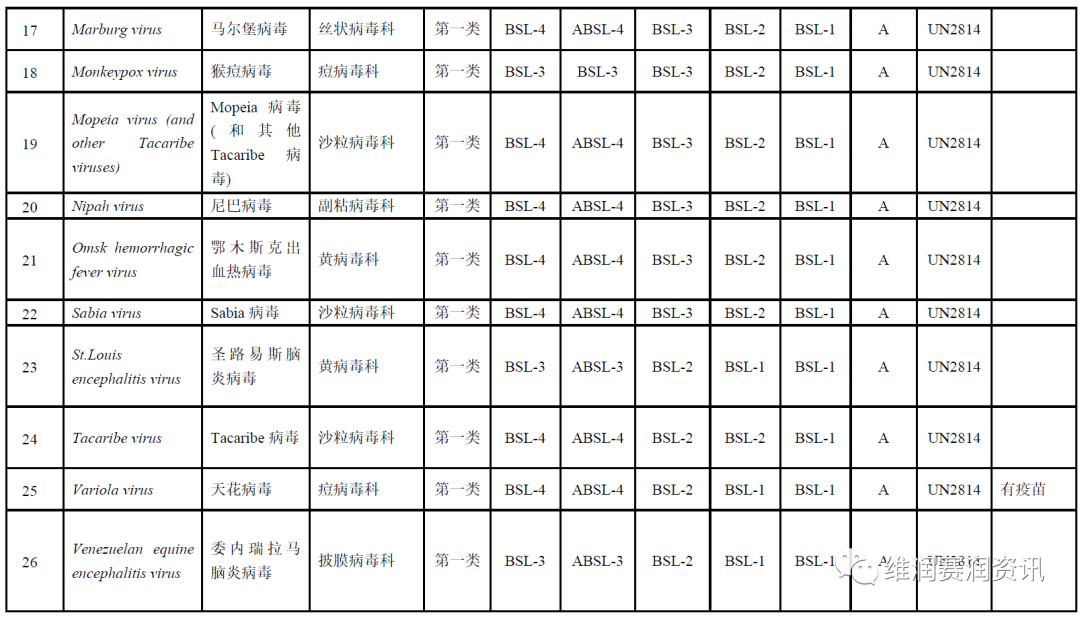
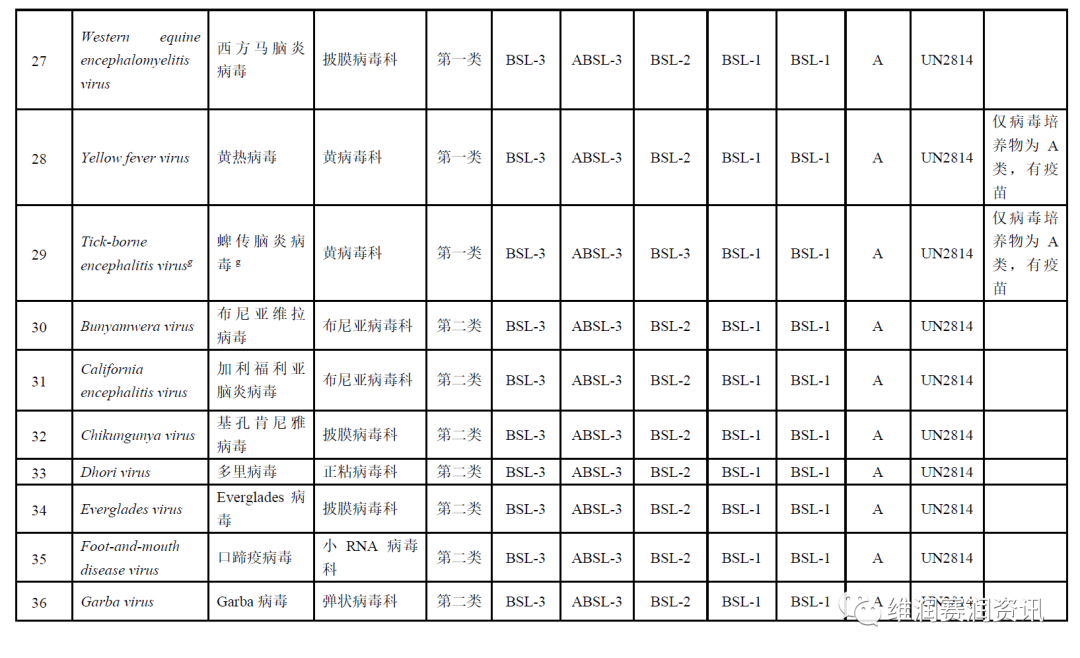
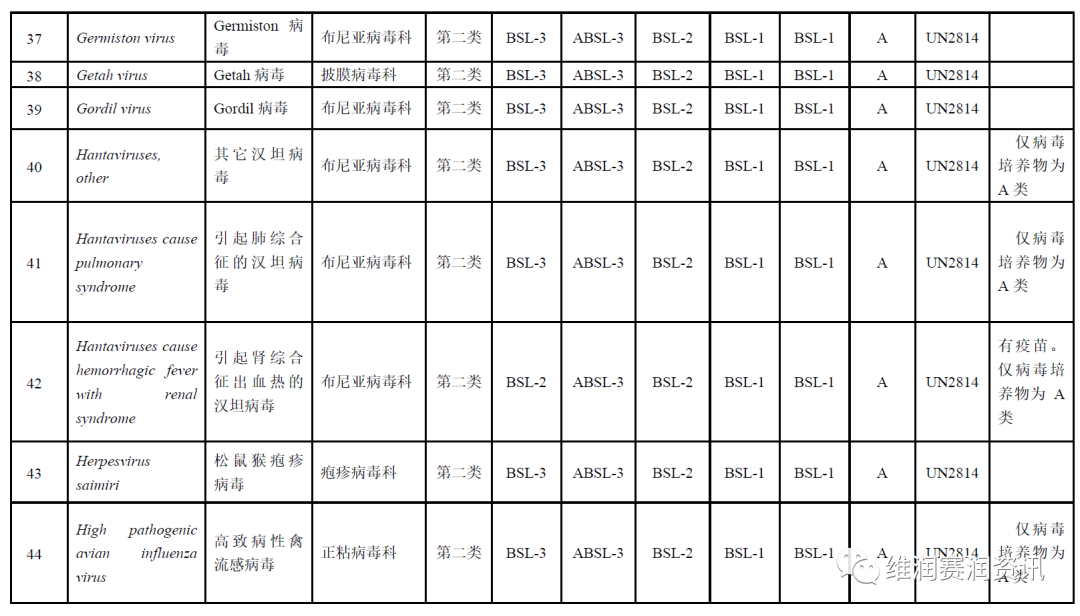
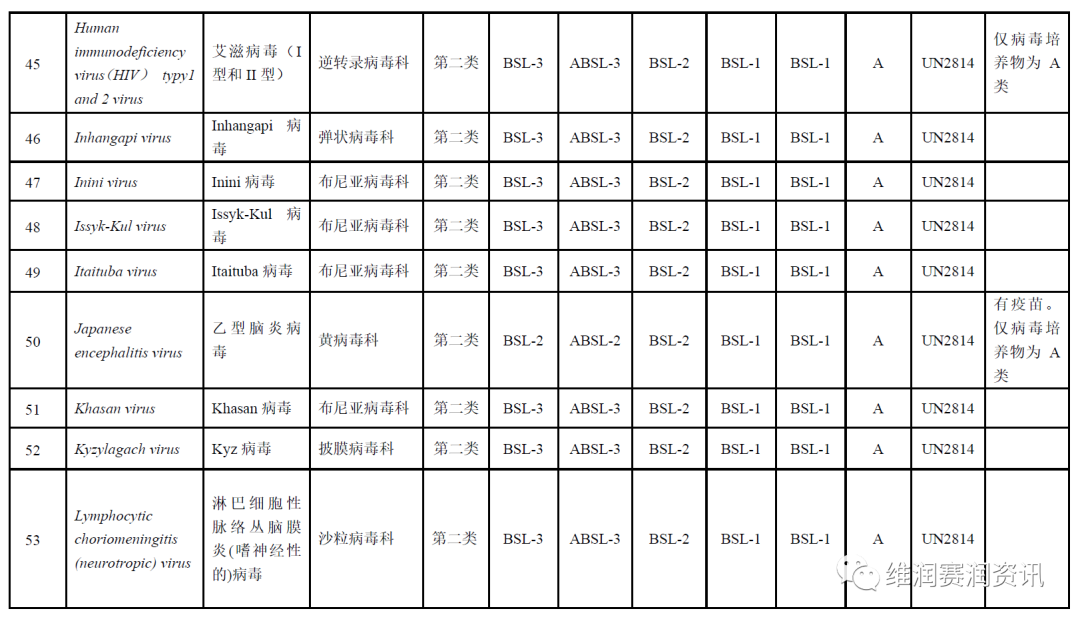
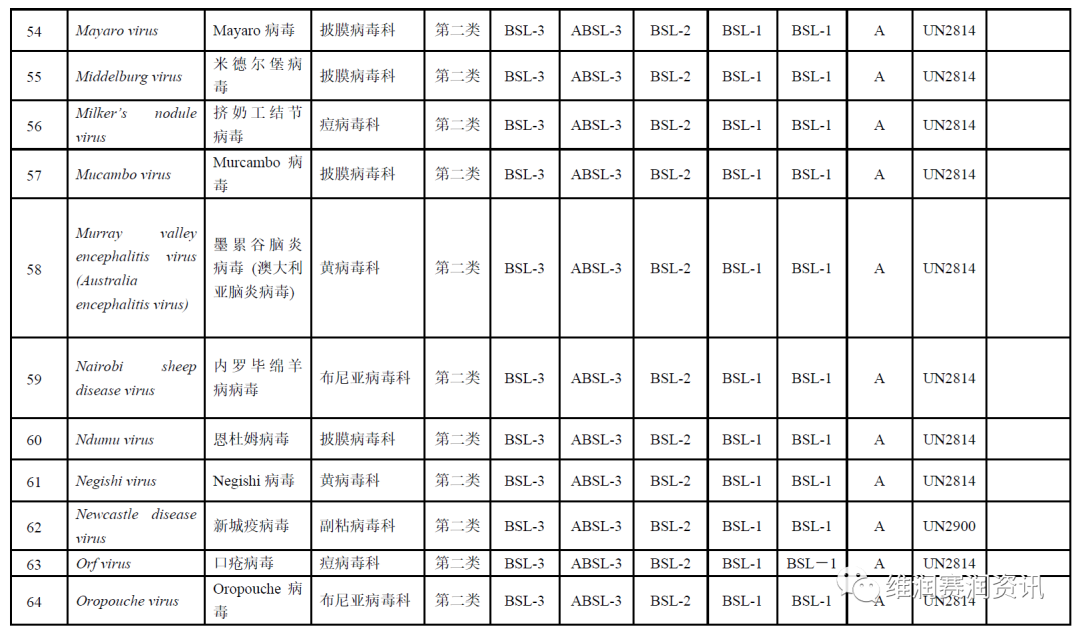
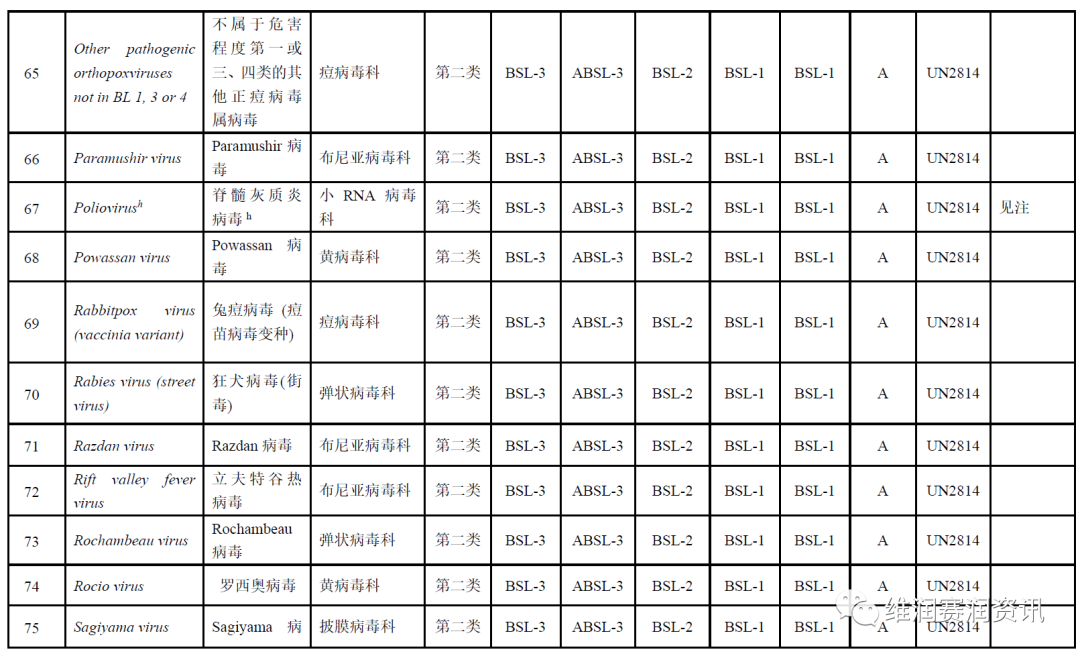
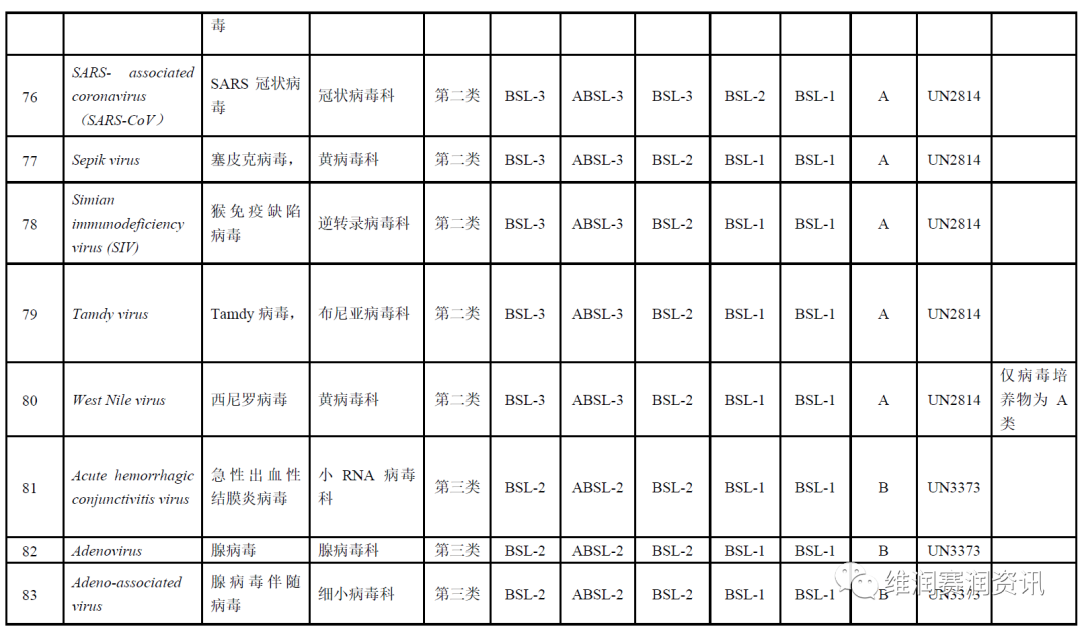
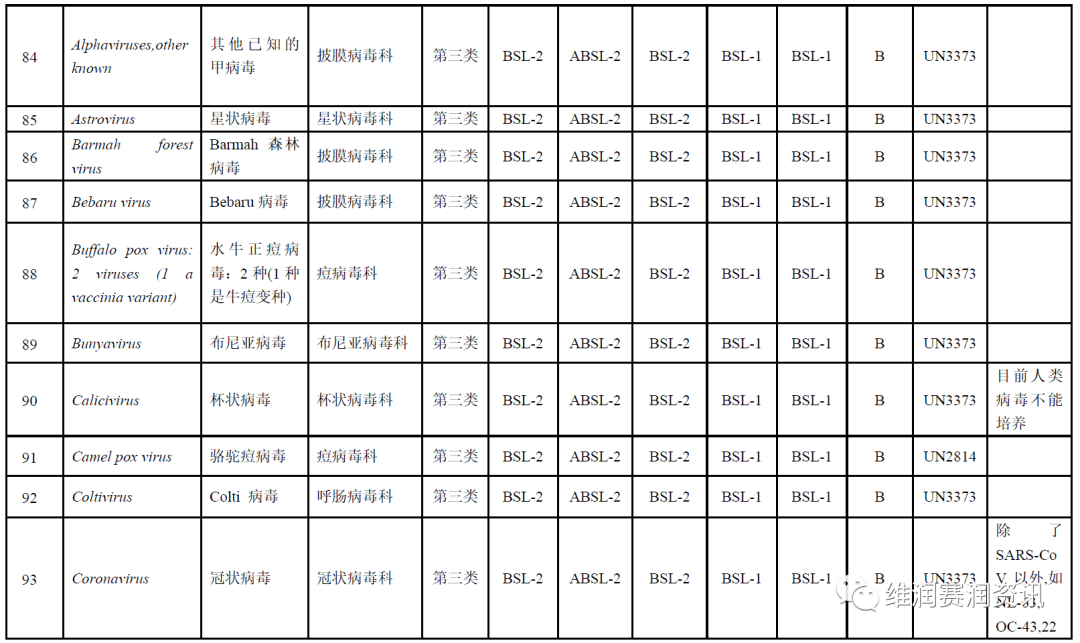
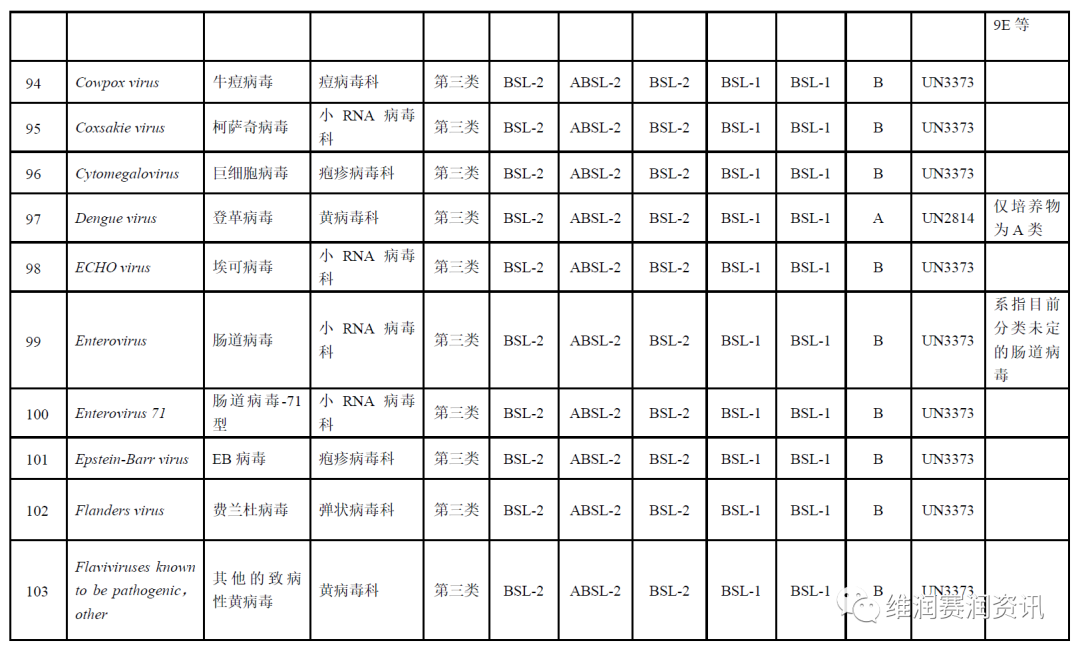
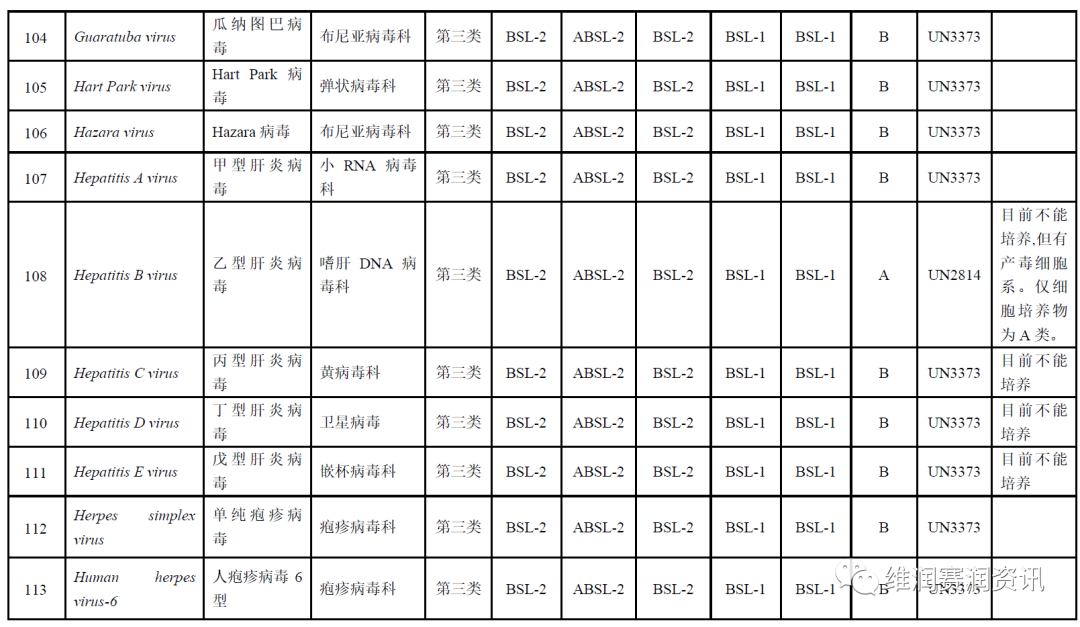
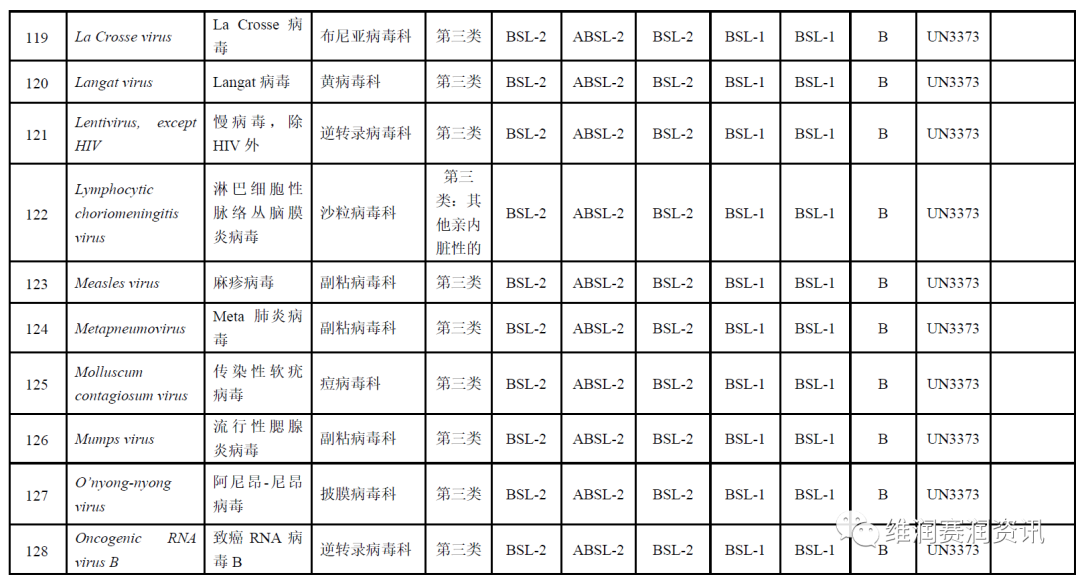
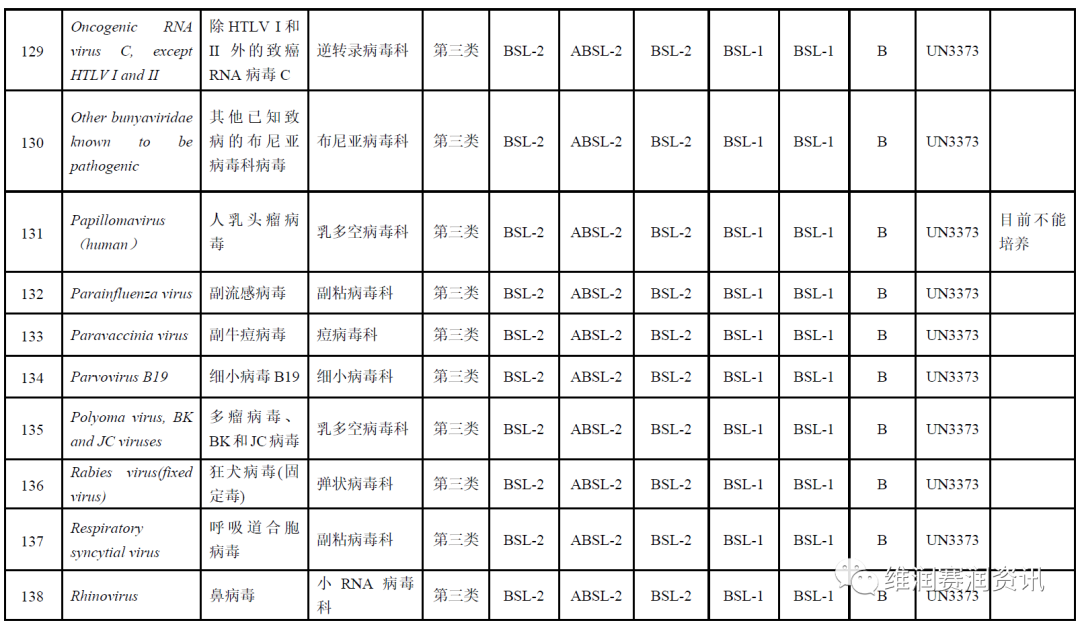
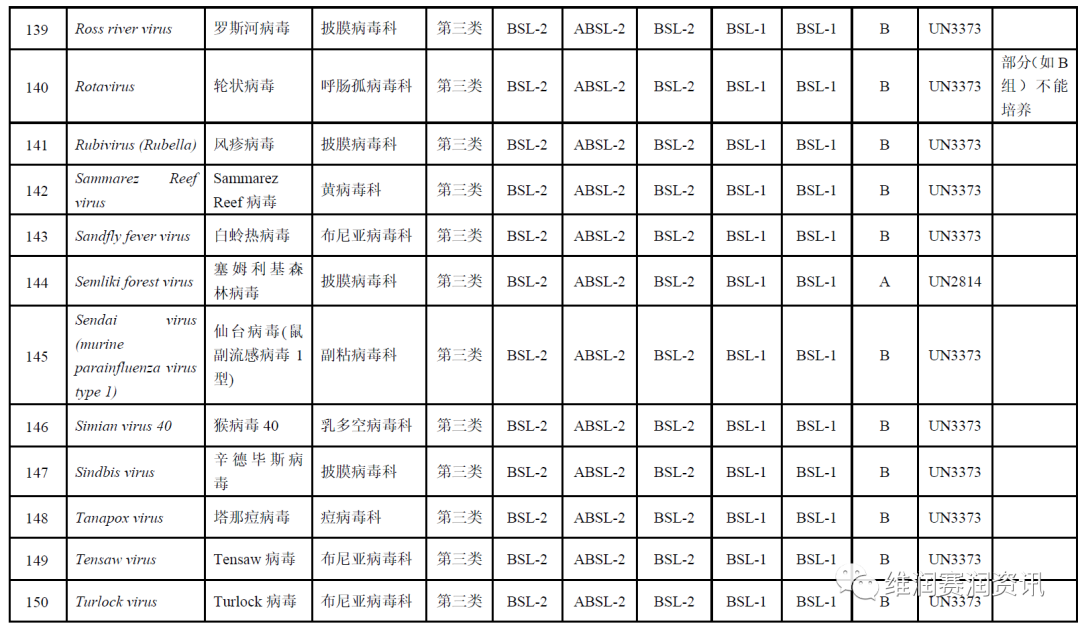
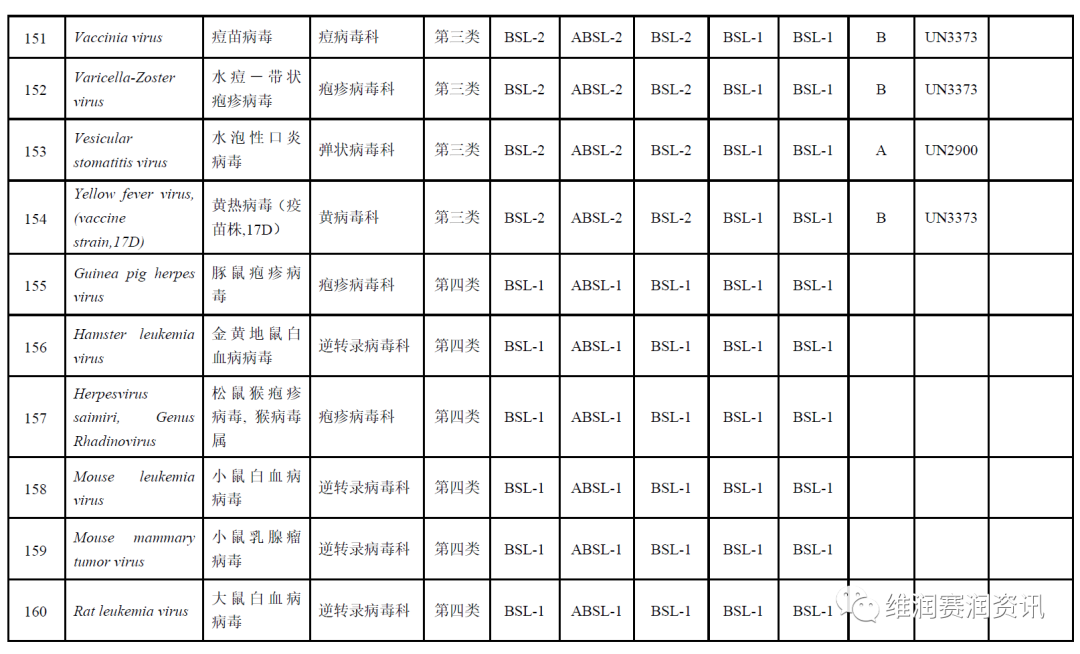
《人间传染的病原微生物名录》——病毒分类名录
数量:160种
SERION SARS-CoV-2抗原为新航海时代赋能!
精雕细琢,工匠精神 ——维润赛润隆重推出“经临床验证”的SARS-CoV-2抗原
划重点 | 《TORCH实验室规范化检测与临床应用专家共识》

国家免疫规划更新,全病毒抗原助攻流行性腮腺炎的检测
药监局开放水痘-带状疱疹病毒检测试剂免临床,virionserion 糖蛋白助力试剂开发
《人间传染的病原微生物名录》——特殊病原体
数量:6种
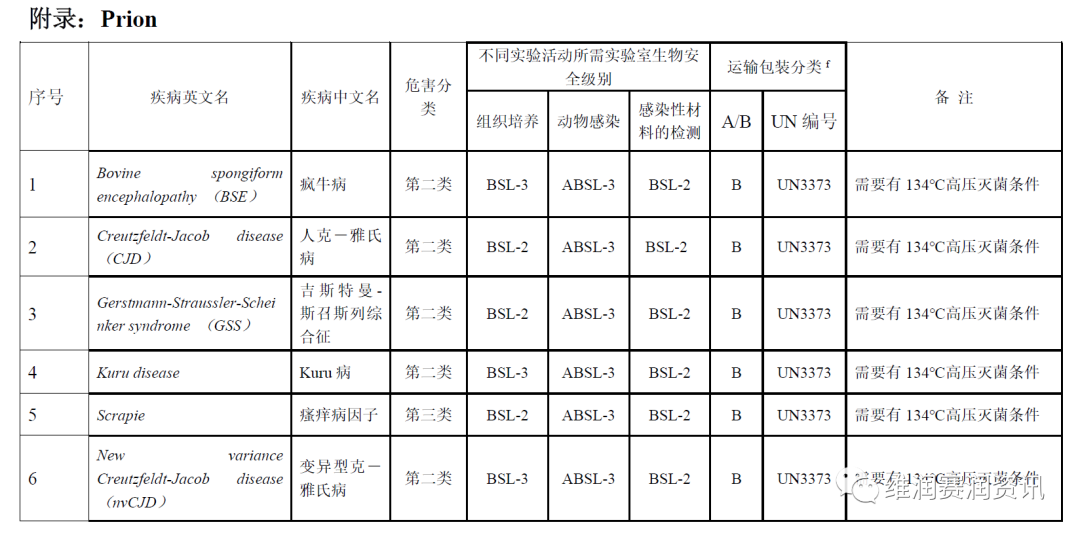
注:BSL-n/ABSL-n:不同生物安全级别的实验室/动物实验室。
a. 病毒培养:指病毒的分离、培养、滴定、中和试验、活病毒及其蛋白纯化、病毒冻干以及产生活病毒的重组试验等操作。利用活病毒或其感染细胞(或细胞提取物),不经灭活进行的生化分析、血清学检测、免疫学检测等操作视同病毒培养。使用病毒培养物提取核酸,裂解剂或灭活剂的加入必须在与病毒培养等同级别的实验室和防护条件下进行,裂解剂或灭活剂加入后可比照未经培养的感染性材料的防护等级进行操作。
c. 未经培养的感染性材料的操作:指未经培养的感染性材料在采用可靠的方法灭活前进行的病毒抗原检测、血清学检测、核酸检测、生化分析等操作。未经可靠灭活或固定的人和动物组织标本因含病毒量较高,其操作的防护级别应比照病毒培养。
d. 灭活材料的操作:指感染性材料或活病毒在采用可靠的方法灭活后进行的病毒抗原检测、血清学检测、核酸检测、生化分析、分子生物学实验等不含致病性活病毒的操作。
e. 无感染性材料的操作:指针对确认无感染性的材料的各种操作,包括但不限于无感染性的病毒DNA或cDNA操作。
f. 运输包装分类:按国际民航组织文件Doc9284《危险品航空安全运输技术细则》的分类包装要求,将相关病原和标本分为A、B两类,对应的联合国编号分别为UN2814(动物病毒为UN2900)和UN3373。对于A类感染性物质,若表中未注明“仅限于病毒培养物”,则包括涉及该病毒的所有材料;对于注明“仅限于病毒培养物”的A类感染性物质,则病毒培养物按UN2814包装,其它标本按UN3373要求进行包装。凡标明B类的病毒和相关样本均按UN3373的要求包装和空运。通过其他交通工具运输的可参照以上标准进行包装。
g. 这里特指亚欧地区传播的蜱传脑炎、俄罗斯春夏脑炎和中欧型蜱传脑炎。
h. 脊髓灰质炎病毒:这里只是列出一般指导性原则。目前对于脊髓灰质炎病毒野毒株的操作应遵从卫生部有关规定。对于疫苗株按3类病原微生物的防护要求进行操作,病毒培养的防护条件为BSL-2, 动物感染为ABSL-2, 未经培养的感染性材料的操作在BSL-2,灭活和无感染性材料的操作均为BSL-1。疫苗衍生毒株(VDPV)病毒培养的防护条件为BSL-2, 动物感染为ABSL-3, 未经培养的感染性材料的操作在BSL-2,灭活和无感染性材料的操作均为BSL-1。上述指导原则会随着全球消灭脊髓灰质炎病毒的进展状况而有所改变,新的指导原则按新规定执行。
说明:
1. 在保证安全的前提下,对临床和现场的未知样本检测操作可在生物安全二级或以上防护级别的实验室进行,涉及病毒分离培养的操作,应加强个体防护和环境保护。要密切注意流行病学动态和临床表现,判断是否存在高致病性病原体,若判定为疑似高致病性病原体,应在相应生物安全级别的实验室开展工作。
2. 本表未列出之病毒和实验活动,由各单位的生物安全委员会负责危害程度评估,确定相应的生物安全防护级别。如涉及高致病性病毒及其相关实验的应经国家病原微生物实验室生物安全专家委员会论证。
3. Prion为特殊病原体,其危害程度分类及相应实验活动的生物安全防护水平单独列出。
4. 关于使用人类病毒的重组体:在卫生部发布有关的管理规定之前,对于人类病毒的重组体(包括对病毒的基因缺失、插入、突变等修饰以及将病毒作为外源基因的表达载体)暂时遵循以下原则:(1)严禁两个不同病原体之间进行完整基因组的重组;(2)对于对人类致病的病毒,如存在疫苗株,只允许用疫苗株为外源基因表达载体,如脊髓灰质炎病毒、麻疹病毒、乙型脑炎病毒等;(3)对于一般情况下即具有复制能力的重组活病毒(复制型重组病毒),其操作时的防护条件应不低于其母本病毒;对于条件复制型或复制缺陷型病毒可降低防护条件,但不得低于BSL-2的防护条件,例如来源于HIV的慢病毒载体,为双基因缺失载体,可在BSL-2实验室操作;(4)对于病毒作为表达载体,其防护水平总体上应根据其母本病毒的危害等级及防护要求进行操作,但是将高致病性病毒的基因重组入具有复制能力的同科低致病性病毒载体时,原则上应根据高致病性病原体的危害等级和防护条件进行操作,在证明重组体无危害后,可视情降低防护等级;(5)对于复制型重组病毒的制作事先要进行危险性评估,并得到所在单位生物安全委员会的批准。对于高致病性病原体重组体或有可能制造出高致病性病原体的操作应经国家病原微生物实验室生物安全专家委员会论证。
5. 国家正式批准的生物制品疫苗生产用减毒、弱毒毒种的分类地位另行规定。
(摘自:人间传染的病原微生物名录)
德国维润赛润提供传染病系列抗原,包括天然抗原与重组抗原,不同形式产品,丰富您的选择菜单。
产品咨询:VirionSerion原料事业部
18818686988 / 0755-89381139
编辑:Steven | 校对:Harris | 责编:Hillson
2021CACLP
原料展馆
N4-S069


助力我们的客户更加强大
永葆我们的价值无可替代
免责声明:本文仅代表作者本人观点,不代表维润赛润资讯的观点和立场。文章图片均来源于网络,如有侵权,请联系作者删除,欢迎联系小编。




























