第十九届中国国际检验医学暨输血仪器试剂博览会(CACLP)
第二届中国国际IVD 上游原材料制造暨流通供应链博览会(CISCE)
CACLP展位号:B5-0805
展会时间:2022 年3 月27 日-3 月29 日
展会地点:南昌绿地国际博览中心
大家好,今天我开始针对免疫诊断试剂的设计、开发和验证,和大家进行一个简单探讨,预计这个系列将会有四篇文章。
做这样一个比较简略的文章,是为了能够为那些研究机构和试剂开发厂商的研究人员、管理人员和质量人员提供一些验证策略和建议,以方便他们能够简单的了解新免疫诊断试剂。
虽然我在这个系列文章中提供了相关的测试和评估参数清单,但是请注意,这不是一个详尽的清单,如果要把这部分完全扩展开来,那就是一门学科,而不是几篇文章所能解决的问题,这也丧失了我们这篇文章的初心,让大家能够简单快速的了解新免疫诊断试剂。
因此,如果读者希望能够对验证方法做进一步的了解,从而确定他们的检测方法是否需要进一步的实验设计和测试的话,请前往阅读《刘博谈》系列,而不是在这个系列文章中寻找答案。
在本系列文章中,我们默认研究/质量人员可以系统地进行实验,按照一种逻辑的方式来验证一种检测方法,并不断记录验证报告所需的数据。同时我们还初步讨论了对诊断试剂有重大影响的因素,如抗体的生产和选择。好了,让我们开始吧。
想象一下,当你被告知自己被检测出患有严重的、危及生命的疾病,但几周后却发现检测结果是假的,在这个过程中,你会受到多大的压力,我有个朋友,在做CA125检测时,就被告知CA125结果异常可能患有癌症,然后哭了一天,花了快一万元进行深入检查,但被最终没有发现什么问题。
这还不是最糟糕的情况,最令人担忧的是,你对这种威胁生命的疾病检测呈阴性,但几个月后却发现你实际上患有这种疾病,而且现在已经发展到威胁生命的晚期阶段。
幸好,和检验实验室相关的法规和质量标准都要求实验室对其所采用的检验方法进行验证,确保不会出现误诊病例,无论是假阳性还是假阴性。
虽然不同的监管组织(如FDA、NMPA、CNAS、ICH、PIC/S、USP、ISO/IEC 170025)提供的验证要求的准则程度有很大差异,但总体目标始终是实现有效的分析测试结果。
使用某一方法的实验室有责任确保该方法得到充分的验证,并且如果有必要,则需要开展进一步的工作来补充现有的数据。例如,如果一个方法已经被一个标准批准组织(如AOAC国际组织)验证,用户通常只需要为他们自己使用该方法建立性能数据。
在其最通用的形式中,免疫诊断试剂是一种依赖于抗体与其目标分析物的特异性结合的分析方法。检测是通过添加信号生成成分(报告标签)来实现的,它可以对目标分析物产生反应。
免疫诊断试剂验证的目的是能够以统计学上可量化的参数来定义测定,并具有测量的信心。只有当它所针对的目标分析物,已经被明确可以用来对不同的疾病类型进行分类,并指导如何采取下一步治疗方案时,该检测方法才有资格被指定为验证的检测方法。
生物分析方法验证包括所有的程序,证明用于定量测量特定生物基质(如血液、血浆、血清、尿液、汗液或乳汁)中的分析物的特定方法对于预期用途是可靠和可重复的。
验证过程(如图1所示)包括通过使用具体的实验室调查,证明该方法的性能特征对于预期的分析应用是合适和可靠的。分析数据是否可以被接受,取决于验证方法的标准,也就是针对其应用场景设定的要求。
图4.1|典型免疫诊断试剂的开发、验证和确认步骤示意图。开发一个检测项目通常从上面显示的检测项目开发和验证步骤开始。这些部分涉及到我们可以称之为开发检测方法的「做出选择」的部分,是定义检测参数的地方。如果该检测方法符合事先确定的分析要求,就可以进行临床前验证,以验证该检测方法是否适用于其预期的目的。这一部分涉及到「确认你做出了正确的选择」,因为它取决于之前做出的决定,如使用的校准模型和样品范围。临床验证是作为已批准的检测方法的持续验证进行的,需要检查该检测方法是否仍然具有预期的功能。
3.1 规划「节约时间要花时间」
在关于更好的战略的5P中,第一个「P」就是规划,这绝不是巧合。规划是任何项目的基础,因为适当的规划可以防止绩效不佳。
免疫诊断试剂可能涉及许多不同复杂程度的步骤和材料,所有这些部件都会给检测带来差异。因此,成功的免疫诊断试剂验证需要一个明确的总计划,以确保验证项目的一致和有效执行。
验证计划应在验证项目启动前和验证实验开始前编写。这个计划可以是一个独立的文件,也可以包含在一个适当的实验室记录中。
该文件应包括对所考虑的免疫诊断试剂的预期用途的描述和对要验证的性能参数的总结。这些参数应包括但不限于精度、准确度、定量范围、标准曲线、特异性和选择性、线性范围、重现性和稳定性。
在检测开发中节省时间的方法之一是花时间计划,啊,其实所有的事都是这样。通过回答下面列出的抗体选择问题(如表1所示),并按照计划执行,这样,研发/质量人员才有可能在减少时间的情况下达到他们的预期目标,并获得一个经过验证的检测方法。
表1|在开发免疫诊断试剂之前需要考虑的重要因素
好了,以上就是今天分享的全部内容,如果大家有什么疑问,欢迎在后台给我们留言,或者加入我们一起讨论~
编辑:Jason | 校对:Harris | 责编:Hillson
公司简介
德国维润赛润(Institut VirionSerion GmbH)成立于1978年,是国际知名的诊断产业原料生产商和供应商。公司的研发和生产基地位于德国维尔茨堡,已通过DIN EN ISO 13485质量体系认证,拥有三级生物安全实验室(P3实验室)。经过了40余年的发展,公司构建了丰富的生物原料产品线,主要包括天然抗原、重组抗原、人源化单克隆抗体和磁珠等。
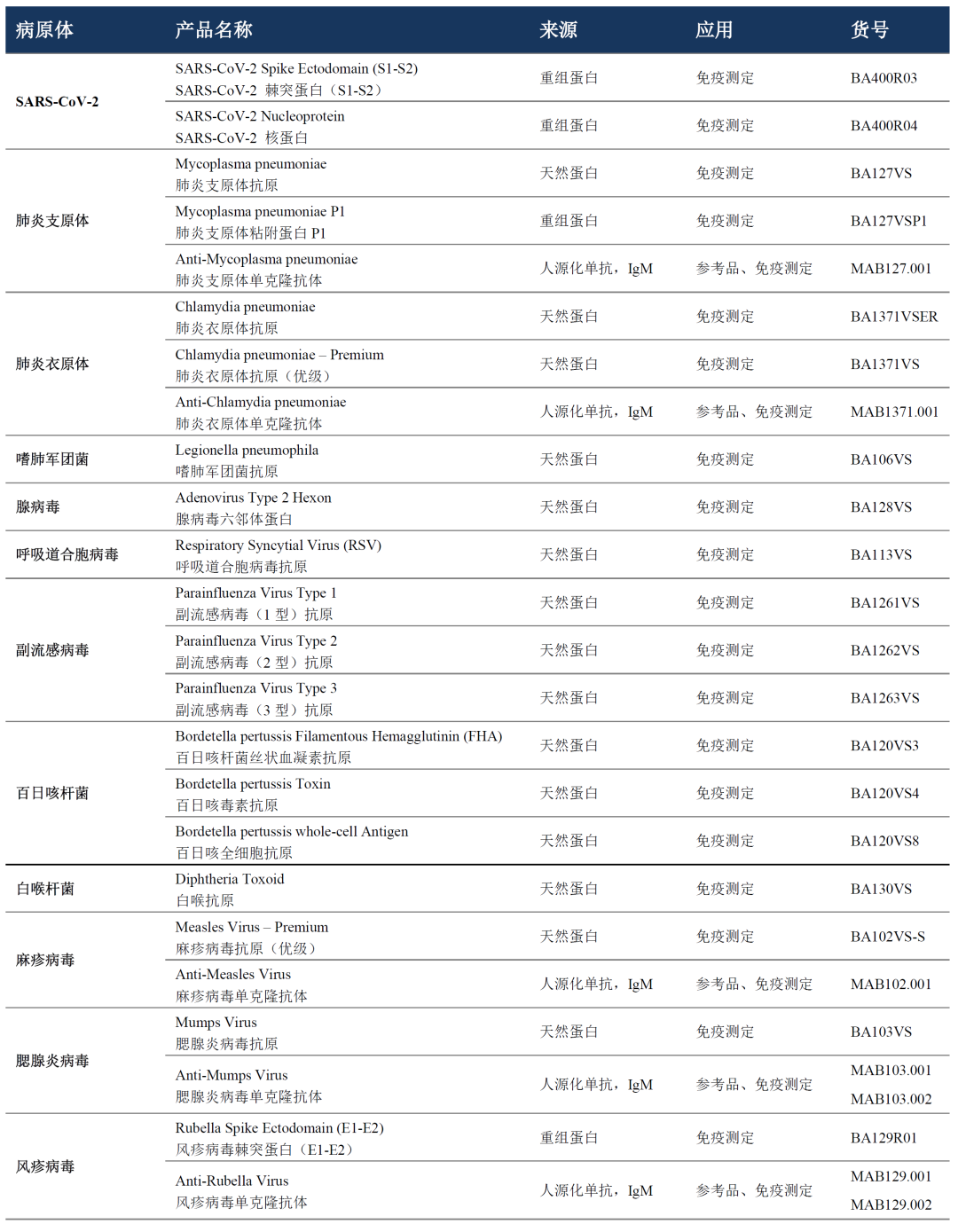
产品信息
产品咨询
SERION原料事业部:
18818686988 0755-89381139

助力我们的客户更加强大
永葆我们的价值无可替代

免责声明:本文仅代表作者本人观点,不代表维润赛润资讯的观点和立场。文章图片均来源于网络,如有侵权,请联系作者删除,欢迎联系小编。












