
通信作者:辛德莉,Email:xindl48@126.com;申昆玲,Email:kunlingshen1717@163.com
作者单位:1首都医科大学附属北京友谊医院,北京热带医学研究所,热带病防治研究北京市重点实验室,北京 100050;2中国医科大学附属盛京医院儿科,沈阳 117004;3清华大学附属第一医院儿科,北京 100016;4首都医科大学附属北京儿童医院呼吸科,北京 100045;5深圳市儿童医院呼吸科,深圳 518034
本文刊发于 中华实用儿科临床杂志,2022,37(16):1252-1256.
引用本文:王良玉,韩晓华,蔚然,等.肺炎支原体实验室诊断方法的临床价值评估[J].中华实用儿科临床杂志,2022,37(16):1252-1256.DOI:10.3760/cma.j.cn101070-20220331-00345.
方法 前瞻性研究。采集2016年12月至2017年1月中国医科大学附属盛京医院临床诊断为MP感染的患儿咽拭子及双份血清;采集2017年3月至5月北京市朝阳区3~5岁健康儿童的咽拭子样本。采用被动凝集法(PA)检测双份血清,以双份血清特异性抗体滴度的4倍升高或降低为金标准,绘制受试者工作特征曲线(ROC),对检测MP感染的实验室方法进行比较和评估。
结果 1.入组临床诊断MP感染患儿93例,其中男42例(45.2%),女51例(54.8%),平均年龄5.5岁,检出确诊MP感染60例(64.5%)。健康儿童349例,男198例,女151例,平均年龄4.3岁,咽拭子样本培养阳性率0.6%(2例),荧光定量PCR(qPCR)检测阳性18.9%(66例)。2.培养特异性最高(100.0%),敏感性最低(65.0%)。PA和酶联免疫吸附试验(ELISA)检测急性期单份血清,敏感性分别为71.7%、86.5%,绘制ROC曲线提示,目前临床采用诊断界值MP特异性抗体IgM≥1∶160并非最佳诊断界值。分子生物学诊断方法敏感性最高,分别为RNA恒温扩增实时荧光检测(SAT)85.0%, qPCR 93.0%;但特异性较低,分别为SAT 75.7%,qPCR 63.6%。3.同时检测患儿咽拭子MP核酸(SAT、PCR)和患儿急性期单份血清(ELISA、 PA),敏感性提升至95.0%~100.0%,特异性63.6%~75.7%。
结论 分子生物学诊断MP感染敏感性高,其存在无症状感染或感染后携带,MP检测阳性,是否需要治疗需结合临床。检测病程1周左右的急性期单份血清敏感性高,对MP感染诊断有参考价值,但确诊需结合临床;采用急性期单份血清学检测方法结合SAT较单独应用检测MP感染的敏感性及准确性高。
1.1 一般资料
1.1.1 实验组 采集2017年3月至5月北京市朝阳区3~5岁幼儿园健康体检儿童的咽拭子样本349例。男198例,女151例,平均年龄4.3岁。入组标准:(1)1个月内无发热、咳嗽等呼吸道感染症状;(2)身高、体质量正常;(3)五官发育良好,无严重视力、听力、口腔等问题;(4)无先天性免疫缺陷及其他系统疾病。
1.1.2 MP感染患儿 采集2016年12月至2017年1月中国医科大学附属盛京医院临床诊断为MP感染患儿93例的咽拭子及急性期、恢复期双份血清。参考菌株选用FH国际标准株(ATCC15531),购自美国ATCC公司。入组标准:(1)发热或无发热,咳嗽(持续剧烈咳嗽为主要表现,无痰或少痰),或伴呼吸困难、喘憋等;(2)肺部听诊音粗或闻及干湿性啰音;(3)血清检测 MP-IgM 抗体、MP-PCR、MP培养,三者之一阳性;(4)胸部X线片无明显影像学改变,或肺部体征较显著,可表现为肺门阴影增重、支气管炎、间质性肺炎、均一的肺实变、肺不张等。排除标准:(1)出现多系统、多器官损害者;(2)患严重肝、肾、心血管及造血系统疾病、免疫系统疾病,以及精神病患儿。将入组患儿分为<3岁组,3~5岁组和>5岁组。本研究通过首都医科大学附属北京友谊医院伦理委员会批准(批准文号:2015-p2-022-01)。
1.2 方法
1.2.1 MP分离培养 接种于胸膜炎微生物(PPLO)培养基,于孵箱内孵育观察,以指示剂颜色变化作为判断MP生长指标。培养基颜色变化后,收集菌株,提取DNA,采用荧光定量PCR(qPCR)扩增DNA并测序,测序结果与基因库DNA序列比对,判定是否为MP。
1.2.2 qPCR检测MP-DNA 采用通用型柱式基因组提取试剂盒(货号CW2298,生产厂家:江苏康为世纪生物科技有限公司)提取基因组DNA,步骤按说明书进行,MP-DNA的检测采用qPCR,SYBR Green 染料法进行qPCR,以反应荧光信号达到阈值时的Ct值作为判定标准,将判定阳性的标本测序,测序结果与基因库对比[4]。
1.2.3 RNA恒温扩增实时荧光检测(simultaneous amplification and testing,SAT) 采用MP核酸检测(RNA恒温扩增)试剂盒(FYM-SAT)(货号:YZB/国3229-2013,生产厂家:上海仁度生物科技有限公司)检测,操作步骤按说明书进行。
1.2.4 酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)检测MP特异性IgM抗体 采用serion ELISA classic肺炎支原体IgM抗体定量检测试剂盒(货号:SCG.AO,生产厂家:Virion\serion德国)检测,操作步骤按照说明书进行。
1.2.5 被动凝集法(passive agglutination,PA)检测血清中特异性抗体滴度 采用赛乐迪亚®-麦可 Ⅱ (SERODIA®-MYCO Ⅱ )(货号:YZB/JAP8033-2013,生产厂家:日本富士瑞必欧株式会社)检测MP混合抗体滴度,操作步骤按照说明书进行。
以双份血清MP特异性抗体滴度的4倍变化为金标准[5]。
1.3 统计学处理 采用SPSS 19.0统计学软件进行数据分析,计量资料以x̄±s表示,计数资料组间的差异比较采用χ2检验或Fisher′s检验,绘制受试者工作特征(ROC)曲线将目前几种实验室检测方法与参考标准进行比较,计算曲线下面积(AUC),评估几种实验室检测方法的临床应用价值。P<0.05为差异有统计学意义。
2.1 健康儿童MP检测情况 健康儿童咽拭子样本349例,qPCR检出MP阳性例数66例,阳性率为18.9%;分离培养2例,阳性率为0.6%。
2.2 MP感染患儿检测情况 患儿93例,其中男42例(45.2%),女51例(54.8%),平均年龄为5.5岁(3~14岁)。咽拭子与急性期血清采集于病程1周左右,恢复期血清采集于病程第2-3周。以双份血清抗体滴度的4倍变化为确诊金标准,男女患儿MP检出率分别为59.5%、68.6%,差异无统计学意义(P=0.361)。3个年龄组患儿男女检出例数(1/6例比2/7例,11/20例比14/21例,13/16例比19/23例)比较,差异均无统计学意义(P=0.612、0.444、0.913)。3个年龄组患儿的MP检出率分别为23.08%、60.98%、82.05%,差异均有统计学意义(<3岁组与>5岁组比较:P<0.001,<3岁组与3~5岁组比较:P=0.017, 3~5岁组与>5岁组比较:P=0.037)。
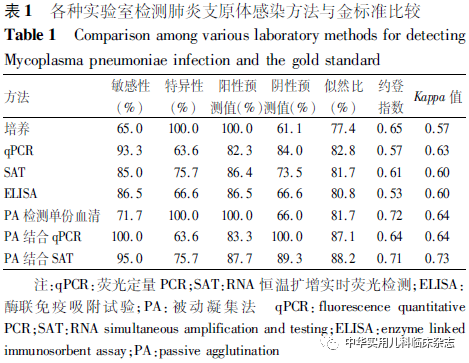
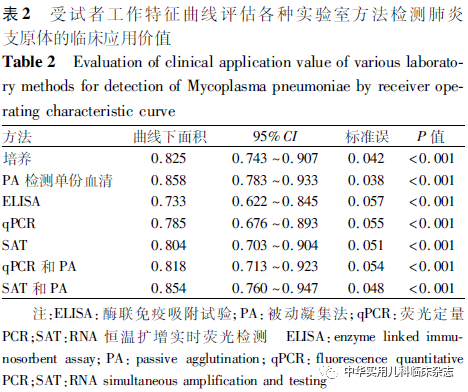
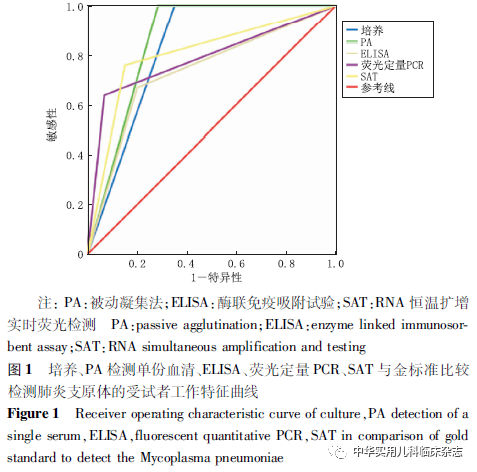
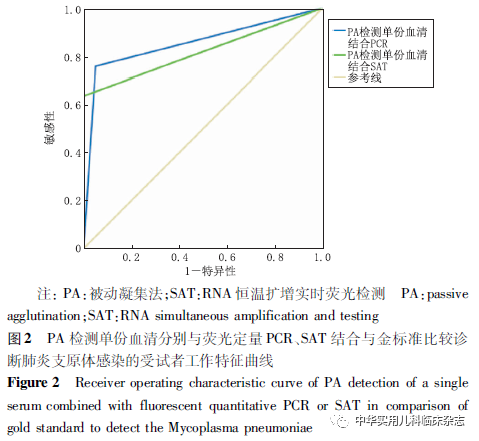
2.3 几种实验室检测方法与参考标准比较 检出MP感染患儿60例(64.5%),培养阳性39例(41.9%),qPCR阳性68例(73.1%),SAT阳性59例(63.4%)。与金标准比较,qPCR敏感性最高(93.3%),特异性较低(63.6%);培养的特异性最高(100.0%),敏感性低(65.0%),易造成漏诊,培养周期为14~21 d,甚至更长,不适于早期诊断。SAT有相对较高的敏感性(85.0%)和特异性(75.7%)。PA检测急性期单份血清,检出阳性43例,敏感性71.7%;PA检测急性期单份血清结合qPCR敏感度提升至100.0%,特异性为63.6%;结合SAT敏感性提升至95.0%,特异性为75.7%,总符合率、约登指数、Kappa值均最高。结果见表1。将培养、PA检测单份血清、ELISA、qPCR、SAT与金标准比较,结果见表2、图1;将PA检测单份血清分别与qPCR、SAT结合,与金标准比较,绘制ROC曲线如图2所示。综合各指标认为检测急性期血清结合SAT为最优诊断方法。
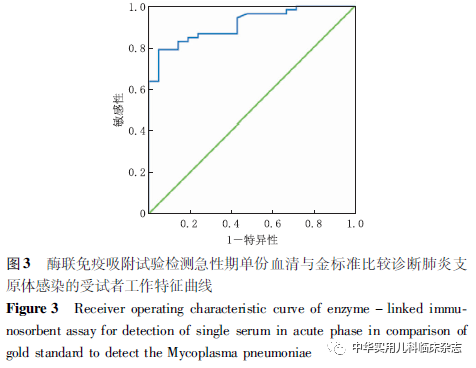
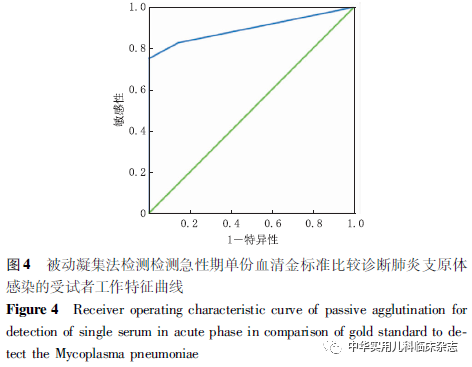
2.4 血清学检测方法的最佳诊断界值 以双份血清4倍升高或下降为金标准,以ELISA方法检测急性期单份血清抗体含量为研究对象,绘制ROC曲线,结果显示阳性界值定为27 U/mL较界值为17 U/mL时(试剂盒设定阳性判定标准)诊断价值略提高(AUC=0.911,P<0.001,95%CI:0.847~0.975)(图3)。以PA检测单份血清抗体滴度为试验组,绘制ROC曲线,结果显示以单次检测血清MP特异性抗体滴度≥1∶160诊断MP感染敏感性略低,以此值为诊断标准,可能会造成漏诊,1∶80 为最佳诊断界值(AUC=0.896,P<0.001,95%CI:0.824~0.967)(图4)。
MP感染是儿童CAP的重要病原,发病率较高,临床表现缺乏特异性,实验室诊断成为明确病原、指导临床用药的重要辅助检查,如何选择早期、快速、准确性高的诊断方法是实验室诊断面临的主要挑战。
MP存在无症状感染或感染后携带现象,本研究采集健康儿童349例咽拭子标本分别进行培养及qPCR,均有阳性检出,无临床症状与机体病原载量及免疫状态相关。国外文献报道MP无症状携带率可达0.1%~56.0%[6]。国内文献报道当MP载量>107 copies/μL才更易引起高热,低载量与发病的关系尚未明确[7-8]。
分离培养特异性高,曾被认为是诊断MP感染的金标准,但因其需要特殊的培养基及实验室条件,生长周期较长,多应用于科学研究。本研究结果显示,培养特异性可达100.0%,但敏感性仅为65.0%,略高于既往文献报道的3%~64%[9],可能与采样时间及本研究入组患儿多为住院患儿有关。本研究MP培养周期为 2~3周,无法满足临床快速诊断的需求。
血清学检测方法是诊断MP感染的常用方法,目前常用的血清学检测方法包括ELISA、PA等,国际上认为双份血清MP特异性抗体4倍升高或降低可确诊MP感染[10-12]。检测双份血清诊断MP感染敏感性可达 39%~88%[13],但2次采血需间隔2周,双份血清采集率较低,无法满足临床快速诊断的需求,因此目前临床多检测急性期单份血清作为临床诊断参考指标。既往研究中检测急性期单份血清敏感性仅约30%[14],本研究中PA检测急性期单份血清敏感性可达71.7%,ELISA法检测急性期单份血清,敏感性为86.5%,明显高于既往报道,考虑与本研究中样本多采集于病程1周左右有关。但文献报道MP感染后抗体可持续阳性数月,既往感染可产生假阳性结果[15];另有文献采用4种商品试剂盒检测102名健康志愿者血清,MP-IgM、MP-IgA也均有阳性检出[16],因此本研究认为临床仅能检测单份血清时,于病程1周左右采集,阳性率更高,但检测阳性并不能作为MP现症感染的确诊依据,是否需要针对MP治疗需结合临床。本研究结果显示,ELISA法与金标准比较,试剂盒所示阳性判定标准低于ROC曲线显示最佳诊断值,单纯采用此方法诊断MP感染存在一定假阳性率,或造成过度诊断。我国关于MP感染诊断的专家共识推荐单次血清检测MP特异性抗体滴度≥1∶160作为MP感染的确诊依据[5],但本研究ROC曲线显示,此界值稍高于最佳诊断点,易造漏诊,考虑原因为本研究样本数较少,建议进一步扩大样本量进行评估。
分子生物学检测方法简单、快速、敏感性较高,对于年龄较小的婴幼儿,分子生物学检测方法更具优势[17]。本研究结果显示,qPCR检测的敏感性、特异性均优于市售试剂盒[18],但特异性仍较低,分析原因为:(1)MP存在无症状感染或感染后携带现象。本研究检测健康儿童,MP检出率为18.9%。国外亦有研究认为MP可在呼吸道存在数月而不引起发病[4]。(2)MP-DNA可在感染后持续检出,长达7周~7个月[19],因此DNA检测阳性不能作为是否需要治疗的依据。本研究选取SAT方法检测MP-RNA,亦有较高的敏感性和特异性,但略低于qPCR。亦有研究显示,SAT与qPCR检测MP有较高的符合率(Kappa=0.97)[20],与本研究存在差异,分析原因认为RNA 较DNA易降解,更易受采样时间保存方式等影响[21],且本研究中入组患儿采样时多数已接受治疗,可能影响MP检出率。检测RNA较DNA特异性提高,可能与RNA较DNA更能反映病原体的生存有关,但本试剂盒检测的为总RNA,而非信使RNA,不能区分现症感染与感染后携带。本研究认为,病程早期分子生物学检测MP感染敏感、快速,符合临床需求,随着病程发展,尤其在应用抗生素后,血清学检测方法较分子生物学更具优势[22]。
血清与分子生物学诊断相结合检测MP感染,是目前学者常推荐采用的诊断方法[22-23]。本研究结果显示,急性期单份血清结合SAT检测MP-RNA,敏感性有较大提高(95.0%),且因RNA易降解,较检测DNA特异性高,诊断的准确性优于单独应用一种方法,为本研究最优诊断方法。
综上,目前实验室检测方法均有各自的局限性,采用任何一种方法诊断MP感染均需结合临床。分子生物学诊断方法特异性相对不足,继续研究MP载量与发病的关系,或能解决此问题。PA检测急性期单份血清可为临床诊断提供参考,探讨单份血清抗体滴度的最佳界值可能有利于提高诊断的敏感性。急性期单份血清结合分子生物学检测方法能提高诊断准确性,建议有条件的单位采用2种诊断方法结合临床综合判断。
参考文献略
(制作:新乡医学院期刊社网络与数字出版部)
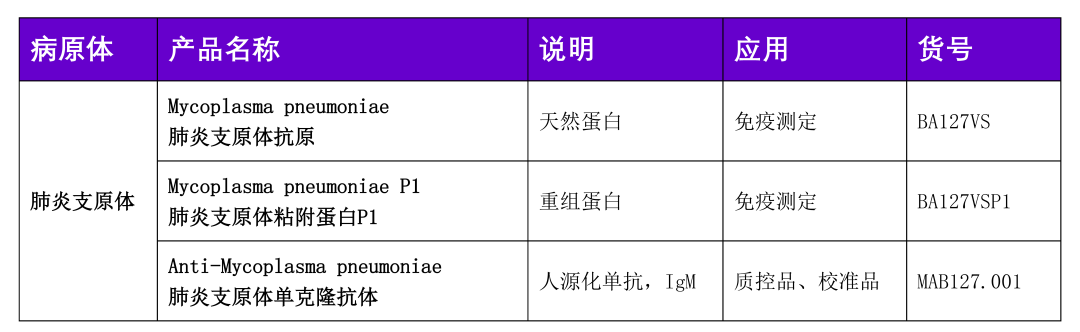
德国维润赛润的肺炎支原体原料清单

公司简介

助力我们的客户更加强大
永葆我们的价值无可替代





