
中华医学会儿科学分会呼吸学组
中国医师协会呼吸医师分会儿科呼吸工作委员会
中国研究型医院学会儿科学专业委员会
中国非公立医疗机构协会儿科专业委员会
中国中药协会儿童健康与药物研究专业委员会
中国医药新闻信息协会儿童安全用药分会
中国初级卫生保健基金会儿科专家委员会
全球儿科呼吸联盟
北京海润公益基金会
通信作者:申昆玲,Email:kunlingshen1717@163.com;钱渊,Email:yqianbjc@263.net
本文刊发于 中华实用儿科临床杂志,2024,39(10):723-732.
引用本文:中国医药教育协会儿科专业委员会,中华医学会儿科学分会呼吸学组,中国医师协会呼吸医师分会儿科呼吸工作委员会,等.中国儿童呼吸道合胞病毒感染诊疗及预防指南(2024医生版)[J].中华实用儿科临床杂志,2024,39(10):723-732.DOI:10.3760/cma.j.cn101070-20240828-00545.
目前国内多项评估RSV感染住院患儿临床和流行病学特征的研究数据公布[4-7]。2023年3月国内首个《人呼吸道合胞病毒感染诊断》团体标准获得批准[8]。2022 年底,Science公布了 2022 年度十大科学突破,其中RSV 疫苗取得突破进展成功入选,标志着 RSV 预防进入了新篇章[9]。
基于当前RSV疾病监测、疾病负担、诊断标准、防治手段等领域的临床证据,制订“中国儿童呼吸道合胞病毒感染诊疗及预防指南(2024医生版)”,以指导和规范我国儿童RSV临床诊疗决策,促进多学科合作,提升我国儿童RSV防控水平。
本指南遵循临床实践指南构建方法学,符合美国医学科学院(institution of medicine,IOM)临床实践指南概念[10],参考 2014 年发布的《世界卫生组织指南制订手册》的制订流程以及相关方法学标准[11],及指南研究与评价工具(appraisal of guidelines for research and evaluation,AGREE Ⅱ)[12] 制订指南计划书和正式指南文件。指南报告参考卫生保健实践指南的报告条目(reporting items for practice guidelines in healthcare,RIGHT)[13]。指南设立指导委员会、制订组、秘书组和外部评审小组。由儿童呼吸科、感染科、新生儿科、保健科医师以及专业期刊编辑、临床流行病学、卫生统计学、病毒学、循证医学、卫生经济学等学科领域的27名专家、学者和研究人员组成,均声明不存在相关经济或非经济性利益冲突。本指南使用人群为各级、各类医疗卫生机构从事儿童呼吸道感染相关工作的临床医师、护士、技术人员及相关科研工作人员;目标人群为5岁以下RSV相关呼吸道感染患者。
本指南通过问卷调研拟定了12个临床问题,检索策略和指南制订方案详见《中国儿童呼吸道合胞病毒感染诊疗及预防指南计划书》[14] ,检索时限均为建库至2023年7月。本指南采用证据推荐分级评估、制订与评价方法(grading of recommendations assessment,development and evaluation,GRADE)系统(表1)对推荐意见的证据质量和推荐强度进行分级,并形成推荐意见[15],综合考虑证据质量、患儿/家长的偏好和价值观、干预措施成本等利弊平衡后共拟定16条推荐意见。于2024年8月11日召开线上专家共识会议,逐条讨论推荐意见、最终达成共识。参考反馈意见进一步修改指南全文,并由5名外部评审专家审定,最后交由指导委员会审核最终定稿。指南工作组将根据证据更新情况,在3~5年内适时启动更新。

RSV属于单股负链病毒目肺病毒科正肺病毒属的成员[16],仅有1个血清型,分为A、B两个亚型。其基因组为非节段性单股负链RNA,全长约15.2 kb,编码11个蛋白质,分别为非结构蛋白NS1和NS2、核衣壳蛋白N、磷蛋白P、基质蛋白M、小疏水蛋白SH 、黏附蛋白G、融合蛋白F、M2-1、M2-2和多聚酶亚单位蛋白L。其中G和F蛋白是RSV膜表面糖蛋白,G蛋白主要负责病毒与宿主细胞黏附,F蛋白介导病毒与宿主细胞膜融合,二者亦是刺激机体产生中和抗体的主要病毒抗原蛋白[17]。F蛋白诱导的中和抗体具有A/B亚型RSV的交叉保护,因此,F蛋白是抗RSV药物和疫苗研发的主要靶蛋白。
同一国家或地区在同一时期可能呈现单一亚型为主或A/B亚型共同流行的特征,且可出现优势亚型的更替[18]。依据G蛋白第2高变区基因特征,RSV 的A和B亚型目前可进一步分为22个和37个基因型[19-23]。A亚型的ON1基因型和B亚型的BA9基因型目前是全球广泛流行的基因型,ON1基因型自2012年在加拿大Ontario地区首次报道后迅速全球流行[24]。我国在2008年前以A亚型GA基因型为主,2010年至2013年以NA1基因型为主,随后ON1基因型取代NA1成为主要基因型[20]。B亚型的BA基因型于2003年首次报道并不断进化,BA9基因型于2005年至2006年在日本首次发现,2006年在我国出现,并于2008年成为我国B亚型中主要流行基因型[20,25-26]。目前我国RSV流行基因型仍以ON1及BA9为主[27-28]。
RSV的流行受地理位置和气候影响。北半球国家主要在11月至次年2月的冬春季流行;热带、亚热带地区潮湿的雨季感染率明显增高[29]。我国北方主要以冬、春季流行为主(10月至次年3月,高峰在11-12月),南北方流行有差异[30-31]。新型冠状病毒疫情期间RSV的流行强度显著降低,疫情后,国外及我国部分城市出现了RSV夏季流行高峰[32-33]。
儿童RSV感染的疾病负担主要是ALRTIs引起的。最近的一项出生队列研究显示,0~24月龄儿童,RSV感染率为0.56次/年,12月龄时40%的儿童至少有1次RSV感染,2岁时达66%[34]。据估计,2019 年在 0~60月龄儿童中,全球约有 3 300 万人次的 RSV 相关 ALRTIs 病例,住院360 万人次,其中 26 300 例 RSV 相关ALRTIs 住院死亡病例,归因总死亡101 200例[1]。
年龄和国家/地区经济发展水平影响RSV相关 ALRTIs 发病率和病死率[1,35]。0~60月龄儿童RSV感染后,大约20%的ALRTIs 病例、39%的住院病例和51%的死亡病例发生在 0~6 月龄婴儿[1];95%以上的RSV 相关 ALRTIs 和97%以上的死亡病例来自低收入和中等收入国家[1]。
据估计我国每年0~60月龄儿童RSV感染引起的ALRTIs发病率约为40.3 (29.7~54.6)/1 000[1],住院率约为(7~11)/1 000,而12月龄以下住院率约为(13~30)/1 000[2]。基于我国30个省份医院网络的研究显示,2009年至2020年期间我国0~60月龄儿童非重症和重症社区获得性肺炎病原中,RSV分别占17.8%和 21.30%,均居第1位[36]。
RSV感染的致病机制较为复杂,涉及病原因素、转录组学、蛋白组学、气道上皮细胞相关因子、免疫系统反应、神经系统反应、宿主因素和环境因素综合作用[37-38]。RSV感染主要累及呼吸系统,其主要机制为气道阻塞、支气管平滑肌痉挛及随后的气道高反应。
3.1 炎症所致气道阻塞 炎症所致气道阻塞是RSV下呼吸道感染的主要致病机制。气管、细支气管和肺泡的上皮细胞是RSV感染的主要靶细胞。RSV感染可引起气道纤毛上皮细胞脱落,脱落的气道上皮细胞与中性粒细胞、纤维素、淋巴细胞在气道中积聚引起气道阻塞,同时黏液的过度分泌及气道的水肿加剧了气道阻塞[39]。中性粒细胞不仅通过释放氧自由基、中性粒细胞弹性蛋白酶、蛋白水解酶损伤气道上皮细胞,还可以通过上调肿瘤坏死因子(tumor necrosis factor,TNF)-α和白细胞介素(interleukin,IL)-13的表达来促使黏液的分泌[40]。RSV感染后机体呈现Th17优势免疫应答,IL-17作为主要的效应因子表达增加,导致大量的黏液产生。
3.2 支气管平滑肌痉挛 支气管及细支气管上皮可因炎性反应受损脱落,导致感觉神经末梢暴露,并释放活性物质,导致支气管平滑肌痉挛;这些递质可反作用于外周靶细胞引起神经源性因子升高,增加感觉纤维的反应性,促进乙酰胆碱、感觉神经肽P物质等的释放,从而增加气道平滑肌细胞(airway smooth muscle cell,ASMC)的收缩幅度。神经肽P物质通过增加ASMC内钙离子浓度,增加ASMC收缩力。同时能激活肥大细胞使其释放组胺、白三烯、IL-6、干扰素(interferon,IFN)-γ及前列腺素D2等,增强收缩支气管作用。
3.3 感染后气道高反应 婴幼儿RSV感染后易发生气道高反应,这与后期的反复喘息和哮喘的发生密切相关。气道高反应的发生与机体的免疫应答、神经调节机制、细胞代谢组学等的改变有关。RSV感染气道上皮后促进Th2和Th17淋巴细胞的分化,呈现Th2、Th17优势免疫应答。Th17优势免疫应答可协同Th2型细胞因子应答增加气道高反应的风险。另外,RSV感染后神经生长因子和神经营养因子受体的表达大量增加,提示RSV感染后的气道高反应可能与气道平滑肌张力的异常神经调控有关[41]。此外,病毒的长期存在可破坏气道微生态平衡,导致气道超微结构的适应性重塑引起气道高反应[42]。RSV感染后会引起代谢组学的改变,如RSV感染促进中长链脂肪酸的扩散和利用,进而扩大氧化损伤和引起促炎细胞因子升高,加重气道高反应[43]。
儿童RSV感染可引起上、下呼吸道感染,不同年龄阶段的临床表现具有差异。小于2岁婴幼儿,特别是6个月龄内婴儿,突出表现为毛细支气管炎或肺炎。病初2~4 d表现为发热、鼻塞和流涕,之后很快出现咳嗽、喘息、呼吸急促等下呼吸道感染症状,可有呼吸费力和喂养困难等。查体可见呼气相明显延长,双肺可闻及广泛弥漫哮鸣音及湿啰音,严重时可出现发绀、鼻翼扇动、胸壁吸气性凹陷、心动过速、脱水等表现。2岁及以上幼儿和儿童多表现为上呼吸道感染,如鼻塞、流涕、咳嗽和声音嘶哑,可有发热;也可表现为气管炎、支气管炎和肺炎等下呼吸道感染[44-46]。
儿童RSV感染也可出现呼吸道外并发症[47-52]。心脏可表现为心肌炎(严重者可发生心力衰竭)、心律失常(室上性和室性心动过速、房室传导阻滞)等;中枢神经系统可表现为惊厥、脑病或脑炎,少见肌张力低下、尿潴留等脊髓受累表现;肝脏可表现为肝炎或肝损害。儿童RSV感染也可合并细菌感染,特别是重症RSV感染[53-54]。
RSV感染后发展为ALRTIs的危险因素包括早产、低出生体重、年龄<6月龄、男性、有兄弟姐妹、母亲吸烟、特应性皮炎史、非母乳喂养和居住环境拥挤等[55];发生重症和危重症的高危人群为早产儿(≤32周)、出生低体重儿、具有支气管肺发育不良、慢性肺疾病、血流动力学改变的先天性心脏病、囊性纤维化、神经肌肉疾病等潜在基础疾病和免疫功能不全的儿童(如原发性免疫缺陷病、移植患儿和人类免疫缺陷病毒感染者)[46]。但健康儿童亦可出现重症甚至危重症临床表现。
实验室检测结果是RSV感染的确诊依据。当前可用于RSV检测的方法包括抗原检测、核酸检测、RSV特异性抗体检测以及病毒分离[56-57]。除了病毒分离,其他3种检查方法在一些发达国家已作为医疗常规[58],目前国内也已有经国家药品监督管理局批准可用于临床检验实验室应用的试剂盒。各种实验室检测方法见表2。
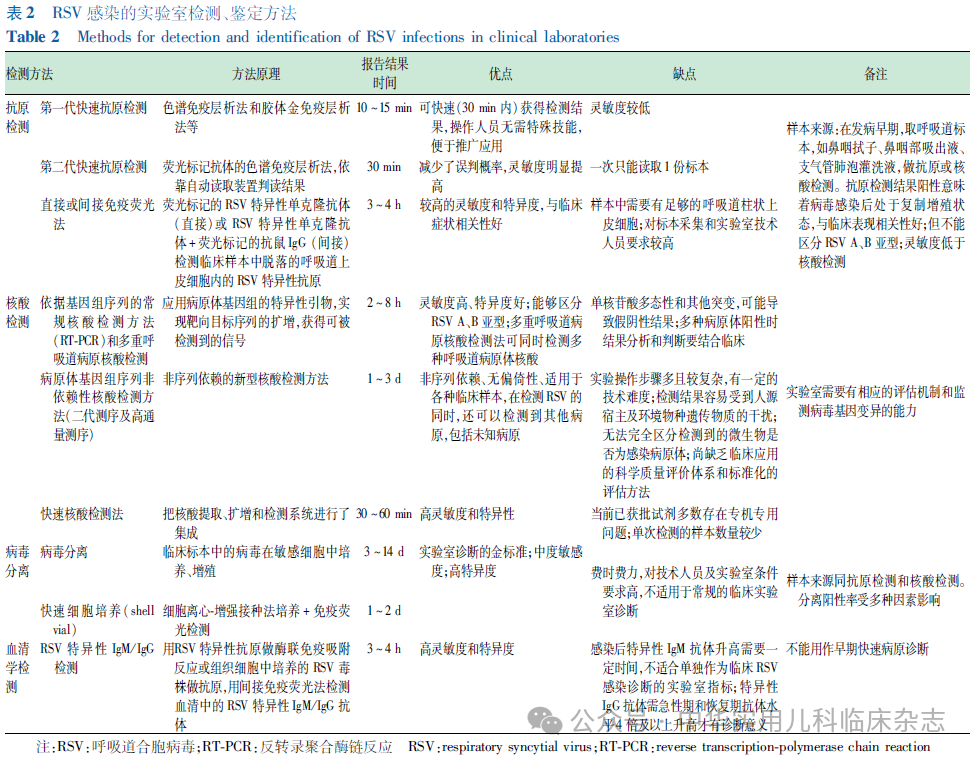
问题1:RSV感染的实验室检测方法如何选择?
推荐意见1:快速RSV抗原检测适用于各级医院的门诊和急诊急性呼吸道感染患儿RSV感染的诊断。
发病早期,抗原阳性可快速做出RSV感染的明确诊断;若抗原阴性,但临床高度怀疑RSV感染,可应用核酸检测进行复核(1A)。
推荐意见2:核酸检测适用于各级医院门诊和急诊,有核酸检测条件的医院可以直接进行核酸检测;多重核酸检测方法适用于住院患儿入院前以及住院后的检测;不推荐应用二代测序(next-generation sequencing,NGS)作为临床常规检测(1A)。
核酸检测的灵敏度和特异度分别为93.5%~100%和近100%,快速核酸检测可将检验报告时限缩短至 1 h。儿童急性呼吸道感染的病原复杂多样[54,59-60],各类病原体引起的儿童急性呼吸道感染常缺乏临床特异性,因此,多重病毒核酸检测能够快速地从呼吸道标本中鉴定出试剂盒所覆盖的呼吸道病毒,有助于病原学鉴别诊断,避免抗菌药物过度应用;为临床分区收治、预防RSV的院内感染提供强有力的依据[61]。在多病原核酸检测阴性,且病情持续进展的情况下,可酌情应用NGS以明确是否有其他或未知病原感染。
推荐意见3:不推荐病毒分离用于RSV感染的常规实验室诊断(1A)。
细胞分离病毒仍然是RSV感染诊断的金标准,具有非常高的特异度,不易受病毒株基因突变影响而出现假阴性结果[62]。但病毒分离培养和毒株鉴定费时(≥16 h)[63],另外RSV具有不稳定特性[56],影响分离阳性率。因此,不推荐病毒分离用于常规临床实验室检测[64]。
推荐意见4:不推荐单份血清RSV抗体作为现症RSV感染的诊断指标(1A)。
RSV可反复感染,多数儿童在2岁后血清中仍可检出RSV的IgG抗体。因此血清学检测无法有效区分急性期感染和既往感染,也无法区分母体来源的抗体。由于反复感染的存在,IgM阳性不能单独作为诊断现症RSV感染的实验室指标[56, 61, 65]。
问题2:RSV下呼吸道感染患儿如何正确氧疗?
推荐意见5:血氧饱和度低于92%,或伴有明显呼吸困难(如吸气性三凹征阳性等)时,推荐给予氧疗(1C)。
血氧饱和度与婴儿毛细支气管炎的住院率和住院时间有关[66-67]。不同研究中启动氧疗的血氧饱和度从90%至95%不等,美国儿科协会2014年版毛细支气管炎诊断治疗预防指南推荐血氧饱和度低于90%时,可以给予氧疗。而意大利2022年毛细支气管炎的指南推荐血氧饱和度低于92%时启动氧疗[46]。我国儿童社区获得性肺炎管理指南(2013修订)及毛细支气管炎诊断、治疗与预防专家共识(2014年版)建议血氧饱和度低于92%时给予氧疗[68-70]。2015年一项来自英国的随机、双盲、平行对照研究发现,经皮血氧饱度低于94%时启动氧疗和经皮血氧饱度低于90%时启动氧疗临床安全性没有区别[71]。
推荐意见6:推荐常规氧疗(standard oxygen therapy,SOT),如有条件优先使用低流量加温加湿氧气吸入。如果效果不好,推荐转为高流量鼻导管吸氧(high flow nasal cannula oxygen inhalation,HFNC)。HFNC治疗失败时需要及时调整为经鼻持续气道正压通气(nasal continuous positive airway pressure,nCPAP),甚至是气管插管机械通气(1A)。
一项前瞻性、随机对照初步研究,包括32名2岁以下毛细支气管炎患儿,给予低流量加温加湿氧气吸入治疗和SOT(鼻导管吸氧2~3 L/min或面罩吸氧5 L/min),两组在呼吸窘迫评分、呼吸频率、住院时长等方面没有显著性差异,但低流量加温加湿氧气吸入可以带来舒适性的提高,临床恢复更快[72]。关于HFNC,一项纳入4项研究1 753例毛细支气管炎患儿的系统综述,比较HFNC与SOT,结果显示在4项随机对照试验中,3项HFNC组的治疗失败率显著低于SOT,而在1项研究中没有发生治疗失败。在SOT失败的情况下,2项样本量最大的试验中,61%的儿童成功转为HFNC,两组有创通气率都非常低,且差异无统计学意义,转入儿童重症监护病房(pediatric intensive care unit,PICU)的比例也没有差异。除了1项PICU的研究外,其他2项研究中两组的氧疗时间和住院时间相似。3项研究(213例)比较了HFNC与nCPAP,2项研究在PICU,1项在普通儿科病房进行。一项研究显示,与nCPAP组相比,HFNC组的治疗失败率更高。而另外两项研究显示,两组治疗失败率很低且相似。气管插管率、机械通气率、PICU住院时间和氧疗持续时间在各组间没有差异[73]。
问题3:重组人IFN-α雾化治疗RSV感染的有效性、安全性如何?
推荐意见7:重组人IFN-α雾化治疗RSV下呼吸道感染安全有效,推荐使用(2C)。
IFN是一类具有广谱抗病毒、抗肿瘤和免疫调节作用的蛋白质,包括 Ⅰ、Ⅱ 和 Ⅲ 型,分别具有不同的受体和功能,是机体天然免疫的关键组成部分。Ⅰ 型IFN包括IFN-α、IFN-β等,IFN-γ是 Ⅱ 型IFN,Ⅲ型IFN包括 IFN-λ2 和IFN-λ3等[74]。
2014年国内的一项多中心随机对照研究,纳入了11家医院330例急性毛细支气管炎患儿,分别使用 2 μg/kg(低剂量组)、4 μg/kg(高剂量组)重组人 IFN-α1b 雾化吸入或常规治疗,2次/d,疗程5~7 d。结果显示低剂量组和高剂量组的总改善率显著优于对照组。高剂量组的主要疗效指标(喘息、喘鸣音、三凹征)的改善率优于低剂量组。RSV阳性患儿主要疗效指标的改善率显著高于RSV阴性患儿。未见呼吸道局部刺激症状,无严重不良反应发生[75]。2020年一项多中心随机非盲法前瞻性研究,纳入来自22家医院675例12月龄以下的毛细支气管炎患儿,分为对照组、肌内注射组(IFN-α1b,10 μg,1次/d)、雾化吸入1组(IFN-α1b,1 μg/kg,2次/d)、雾化吸入2组(IFN-α1b,2 μg/kg,2次/d)4个组。雾化吸入重组人IFN-α1b组在咳嗽评分、喘息改善等方面有明显改善(高剂量组改善更明显),未报道严重不良反应[76]。另一项随机对照多中心研究,雾化吸入人重组人IFN-α2b,低剂量组10万IU/(kg·次)、高剂量组20万IU/(kg·次),2次/d,与对照组比较,可显著提高急性毛细支气管炎患儿的治愈率、有效率,缩短症状消失时间、总病程,高剂量组更优,安全性较好[77]。
雾化吸入剂量和疗程:IFN-α1b 2~4 μg/(kg·次),2次/d;IFN-α2b 10万~20万IU/(kg·次),2次/d;疗程 5~7 d。
问题4:RSV下呼吸道感染患儿如何正确使用糖皮质激素?
推荐意见8:对于第1次患毛细支气管炎既往健康的婴幼儿,不推荐使用全身或吸入糖皮质激素(1A)。有特应性个人史或家族史的喘息患儿可以试用(2D)。
2014年一项关于糖皮质激素治疗婴幼儿病毒性毛细支气管炎的系统综述,纳入了17项临床随机试验(包括2 596例2岁以下急性毛细支气管炎患儿),对比短期使用全身糖皮质激素或吸入糖皮质激素与安慰剂之间的差异,结果显示使用全身或吸入糖皮质激素均不能缩短住院时间和改善症状严重程度[78]。有特应性个人史的儿童,RSV感染后出现反复喘息和哮喘的风险较高。在充分评估利弊的基础上可以试用,并加强随访观察。
问题5:RSV下呼吸道感染患儿如何正确使用支气管舒张剂?
推荐意见9:不推荐支气管舒张剂用于RSV下呼吸道感染的常规治疗(1B)。有特应性个人史或家族史的患儿,可试用以改善气道阻塞症状(2D)。
2014年一项系统综述,分析了来自30项临床研究(包括1 992名毛细支气管炎婴儿),支气管舒张剂组和安慰剂组相比,在住院率和住院时间上没有差异[79]。但这些研究存在相当大的异质性,样本量小,缺乏标准化的验证结果,因此需要更高质量的研究去验证。2019年英国一项关于毛细支气管炎管理和预防的更新综述指出,尽管不建议常规使用吸入性支气管舒张剂,但一小部分毛细支气管炎患儿,尤其是有哮鸣音而无湿啰音,和/或有特应性个人或家族史的患儿,可能会对支气管舒张剂治疗有反应[80]。
问题6:痰液黏稠患儿是否需要祛痰治疗?如何正确选择祛痰药物?
推荐意见10:伴有明显气道高分泌的患儿可酌情使用祛痰药物(如雾化N-乙酰半胱氨酸溶液,雾化、口服、静脉滴注盐酸氨溴索等),用药时应注意监护患儿有无气道梗阻和/或呼吸困难(2C)。
在RSV引起的下呼吸道感染患儿中,尚未见高质量多中心临床研究证明祛痰药物的适应证及使用方法。巴基斯坦的一项单中心随机对照研究雾化N-乙酰半胱氨酸溶液对儿童急性毛细支气管炎的疗效,结果显示雾化N-乙酰半胱氨酸溶液可以改善临床严重程度和缩短住院时间[81]。一项纳入2 076例>6月龄的急性肺炎患儿的多中心前瞻性研究显示,雾化吸入盐酸氨溴索治疗7 d,咳嗽改善率为 96.87%,喉中痰鸣音改善率为90.46%,肺部听诊改善率为84.59%;随用药时间延长,咳嗽症状、喉中痰鸣症状以及肺部听诊体征均呈好转趋势。未见严重不良反应[82]。
部分患儿由于呼吸增快不显性失水增加,病情重或持续咳嗽等影响经口摄入,加重痰液黏稠,因此保证足够的液体入量,维持水电解质平衡,对毛细支气管炎的治疗也非常重要[83]。
问题7:RSV下呼吸道感染患儿是否需要高渗盐水雾化治疗?
推荐意见11:不推荐3%高渗盐水雾化吸入作为RSV下呼吸道感染住院患儿的常规治疗(2C)。
2023年更新的雾化高渗盐水溶液治疗婴儿急性毛细支气管炎的系统综述,共纳入34 项随机对照试验和准随机对照试验,5 205例婴儿,其中 2 727 例接受了雾化高渗盐水(3%~7%)治疗,对照组为雾化0.9%生理盐水或常规治疗。在住院婴儿中,接受雾化高渗盐水的平均住院时间较接受0.9%生理盐水或常规治疗的患儿缩短0.4 d(95%CI:-0.69~-0.11;21 项试验,2 479 例婴儿;低质量证据)。在门急诊婴儿中,与雾化生理盐水相比,雾化高渗盐水可使住院风险降低 13%(RR=0.87,95% CI:0.78~0.97;8项试验,1 760例婴儿;低质量证据)。13项试验[2 792例婴儿;1 479例使用雾化高渗盐水治疗,其中1 063例(72%)单独使用雾化高渗盐水,416例(28%)联合支气管舒张剂]报告了至少 1项不良事件,包括咳嗽、烦躁、支气管痉挛、心动过缓、血氧饱和度下降、呕吐和腹泻,其中大多数是轻微的,可自行缓解(低质量证据)。所有结果均为低或极低质量证据,且存在不一致性和偏倚风险[84]。
问题8:RSV下呼吸道感染患儿是否需要使用免疫球蛋白?
推荐意见12:不推荐免疫球蛋白作为RSV下呼吸道感染患儿的常规治疗(1B)。
2023年的系统综述纳入了8个临床试验(包含906名3岁以下RSV感染婴儿),这些试验中使用的免疫球蛋白制剂包括普通免疫球蛋白、抗RSV免疫球蛋白、帕丽珠单抗和莫塔韦珠单抗。结果显示在常规住院时间、需要机械通气及氧疗时间、需要转PICU的比例、PICU住院时长、不良反应等方面,免疫球蛋白治疗组和安慰剂组无显著差异[85]。
问题9:RSV感染患儿何时需要使用抗菌药物?
推荐意见13:不推荐常规使用抗菌药物(1B)。需要气管插管和机械通气者合并细菌感染可能性增大,或有足够证据表明合并细菌感染者可酌情使用抗菌药物(1D)。
国内外指南/共识均不建议RSV感染治疗中常规使用抗菌药物,除非有足够的证据表明有细菌感染存在[46, 70, 83]。2014年一项系统综述分析包含7项临床随机对照研究(包括824名2岁以下毛细支气管炎患儿),结果显示没有足够证据支持常规使用抗菌药物(阿莫西林、氨苄西林、克拉霉素、阿奇霉素、红霉素等)。抗菌药物可用于伴发或继发细菌性肺炎的病例[86]。Thorburn等[87]报道165例<6月龄入住PICU的重症RSV毛细支气管炎患儿,42.4%的患儿下呼吸道分泌物细菌检测阳性。呼吸衰竭、需要气管插管和机械通气者合并细菌感染可能性增大[88-89]。
问题10:RSV感染患儿是否需要使用白三烯受体拮抗剂?
推荐意见14:不推荐白三烯受体拮抗剂作为RSV下呼吸道感染患儿的常规治疗(2B)。有特应性个人史或家族史伴有明显喘息的患儿,可能会有临床获益(2D)。
2015年一项系统综述纳入了5项随机对照临床试验(包括1 296名24月龄以下因毛细支气管炎住院的婴儿),结果不能就使用白三烯受体拮抗剂对毛细支气管炎婴幼儿住院时间和临床严重程度评分的影响得出明确结论[90]。由于研究的异质性和可信区间比较大,将来需要进一步大样本同质性的研究。2010年一项双盲随机对照研究,纳入了200例首次RSV感染后的6月龄至2岁患儿,分为孟鲁司特治疗组(4 mg,1次/d)、安慰剂和空白对照组,治疗3个月,结果显示孟鲁司特治疗组(79例)血清嗜酸性粒细胞衍生神经毒素水平显著降低(P<0.01),随诊12个月时,孟鲁司特治疗组的累计反复喘息发作次数显著减少(P=0.039)[91]。
7.1 非药物干预措施
7.1.1 社区预防 加强对RSV感染及防治方面的宣教;提倡母乳喂养至少至6月龄[83];避免暴露于烟草和其他烟雾;在RSV流行季节,增加环境通风[92],限制高风险婴儿去儿童保育机构[83];应勤洗手(用肥皂洗手或含酒精的溶液洗手)、戴口罩,尤其是高风险婴儿在暴露于有呼吸道感染风险的年长儿童时[93-94];养成良好的咳嗽卫生习惯。鼻腔冲洗能够降低上呼吸道病毒载量,减少病毒飞沫或气溶胶向空气中释放[95-97]。物体表面消毒可选用浓度为 0.1%的次氯酸钠或70%~90%的酒精[98]。
7.1.2 医院预防 与RSV感染患儿直接接触的人员均应在接触患儿前后消毒双手,如无法使用乙醇类消毒剂,应用肥皂和水洗手,并使用个人防护用品;推荐尽可能将患儿隔离于单人病房或与其他 RSV 感染者一起隔离于同一病房(集中隔离治疗),并限制将患儿转出病房。在RSV感染流行期间,应尽量避免照顾 RSV 感染者的医护人员同时照顾非RSV感染患儿;医务人员应持续接受相关教育,包括 RSV 感染的症状、流行病学、诊断和传播[99-102]。
7.2 RSV特异性单克隆抗体预防
问题11:尼塞韦单抗(Nirsevimab)的适用人群有哪些?其预防RSV感染的安全性及有效性如何?
推荐意见15:推荐RSV流行季节出生的新生儿和即将进入第1个RSV流行季节的婴儿注射尼塞韦单抗,预防RSV引起的下呼吸道感染(1A)。
美国最新的真实世界数据显示尼塞韦单抗降低婴儿因RSV住院的风险达90%,西班牙多个地区的真实世界研究也观察到,注射尼塞韦单抗后减少了近90%的婴儿RSV感染住院率[103-104]。尼塞韦单抗的安全性良好,大多数病例的不良反应严重程度为轻度至中度,常见的不良反应包括皮疹(0.7%)、发热(0.5%)和注射部位反应(0.3%),均为偶见(≥1/1 000至<1/100),注射部位反应均不严重[105]。真实世界数据显示尼塞韦单抗安全性与产品说明书总体保持一致[103-105]。
RSV感染属于自限性疾病,绝大多数感染患儿预后良好,不遗留后遗症。极少数患儿出现呼吸衰竭、神经系统并发症,甚至死亡。少数患儿感染后期可出现反复喘息、支气管哮喘,部分遗留感染后闭塞性细支气管炎等。
问题12:RSV感染后是否需要长期随访?
推荐意见16:推荐RSV感染后长期随访,特别是2岁前感染RSV的婴幼儿(1A)。
婴幼儿期RSV感染,特别是严重的RSV感染是学龄前儿童发生反复喘息和儿童期发生哮喘的高危因素。一项队列研究纳入68 130名婴儿,其中30.7%曾因RSV住院,长期随访显示,这些患儿反复喘息或哮喘的累积发病率高于非RSV感染者。推测RSV住院治疗与之后的反复喘息和哮喘有关,且主要在学龄前儿童[106]。一项包括47项研究的Meta分析显示,与未感染RSV的婴儿相比,感染RSV的婴儿更容易出现喘息(OR=3.12,95%CI:2.59~3.76),且在康复后出现喘息性疾病的风险更高(OR=2.60,95%CI:2.51~2.70)[107]。一项回顾性队列研究对 23 365 名儿童进行了中位数 6.9 年的随访,将2岁前RSV呼吸道感染的儿童作为暴露组,同龄意外事故儿童为对照组。结果显示RSV感染与哮喘和喘息的关联在前2年最强,随时间减弱;在6~23月龄首次感染RSV的婴幼儿,关联可持续6年;而在6月龄以下首次感染RSV者,关联仅在最初2年显著。表明6~23月龄首次感染RSV婴幼儿更易随后出现喘息和哮喘[108]。
RSV感染的治疗和预防一直是研究热点。特异性抗RSV感染治疗药物研发取得进展,齐瑞索韦(Ziresovir)完成 Ⅱ 期临床试验。疫苗(Abrysvo)在国外获批用于孕妇以预防婴儿出生后6个月内的RSV感染[109]。儿童可以使用的疫苗在研发中。尼塞韦单抗的临床使用,将减少婴幼儿RSV感染和住院,减轻RSV疾病负担。
徐保平和谢正德对本文有同等贡献
参与本指南制定和审校的专家(按姓氏拼音排序):曹玲(首都儿科研究所附属儿童医院);陈祥鹏(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);邓继岿(深圳市儿童医院);杜立中(浙江大学医学院附属儿童医院);方海(北京大学中国卫生发展研究中心);符州(国家儿童健康与疾病临床医学研究中心,重庆医科大学附属儿童医院);李昌崇(温州医科大学附属第二医院/育英儿童医院);李建华(中华实用儿科临床杂志);李有(南京医科大学公共卫生学院);刘瀚旻(四川大学华西第二医院);刘雅莉(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);卢根(广州医科大学附属妇女儿童医疗中心);彭晓霞(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);钱渊(首都儿科研究所);秦强(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);任丽丽(中国医学科学院&中国协和医学院病原生物学研究所);尚云晓(中国医科大学附属盛京医院);申昆玲(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心,深圳市儿童医院);孙丽红(广州医科大学附属第一医院);王健伟(中国医学科学院,北京协和医学院);谢正德(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心,中国医学科学院儿童危重感染诊治创新单元);徐保平(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);张海邻(温州医科大学附属第二医院/育英儿童医院);张燕(中国疾病预防控制中心病毒病预防控制所);赵林清(首都儿科研究所);郑跃杰(深圳市儿童医院)
参与本指南外审的专家(按姓氏拼音排序):安淑华(河北省儿童医院);韩志英(山西省儿童医院);李明(昆明市儿童医院);刘长山(天津医科大学第二医院);孙欣荣(西安交通大学附属儿童医院)
德国维润赛润呼吸道合胞病毒(RSV)原料清单


公司简介

德国维润赛润(Institut VirionSerion GmbH)成立于1978年,是国际知名的诊断产业原料生产商和供应商。公司的研发和生产基地位于德国维尔茨堡,已通过DIN EN ISO 13485质量体系认证,拥有三级生物安全实验室(P3实验室)。经过了40余年的发展,公司构建了丰富的生物原料产品线,主要包括天然抗原、重组抗原、人源化单克隆抗体和磁珠等。
助力我们的客户更加强大
永葆我们的价值无可替代

免责声明:本文仅代表作者本人观点,不代表维润赛润资讯的观点和立场。文章图片均来源于网络,如有侵权,请联系作者删除,欢迎联系小编。



