
本文转载自微信公众号“检验医学”(labweb)
TORCH指一组病原体,包含弓形虫、风疹病毒、巨细胞病毒、单纯疱疹病毒等,孕妇感染此类病原体后可通过胎盘或产道感染胎儿或者新生儿,可能导致流产、早产、畸胎、死胎、宫内发育迟缓、新生儿多器官损害等不良预后。
因为目前尚缺乏有效的治疗手段,所以加强产前TORCH感染监测非常重要,但一直以来TORCH筛查常常给临床带来一些困扰。诸如:孕妇是否感染,是什么时候感染?胎儿是否被感染,是否会发生先天性畸形?甚至有仅凭TORCH-IgM阳性,就武断建议流产的痛心案例,同时,多学科联合评估的缺失,难以判断孕妇感染与胎儿感染的相关性、胎儿感染与出生结局的相关性。究其原因:
由尚世强主任、朱宇宁主任、陈英虎主任等24位来自全国妇幼、儿童系统的检验、临床专家联合撰写的《TORCH实验室规范化检测与临床应用专家共识》发表于2020年5月43卷第5期的《中华检验医学杂志》。
共识基于TORCH检测方法特点,针对不同病原体的感染特点、感染类型,从实验室角度对TORCH规范化检测与临床应用给出了共识性意见。
TORCH血清学检测方法
目前是临床首选
TORCH临床实验室检测的主要手段包括血清学和病原学检测。共识强调TORCH血清学检测方法简便、操作标准化、成本较低,目前是临床首选的检测方法,检测指标包括特异性免疫球蛋白M抗体、特异性免疫球蛋白G抗体和IgG抗体亲和力等。这与2016年至2020年国家卫健委临检中心TORCH室间质评上报实验室数据(以巨细胞CMV-IgM为例)中呈现出TORCH血清学检测实验室家数逐年增加趋势一致。
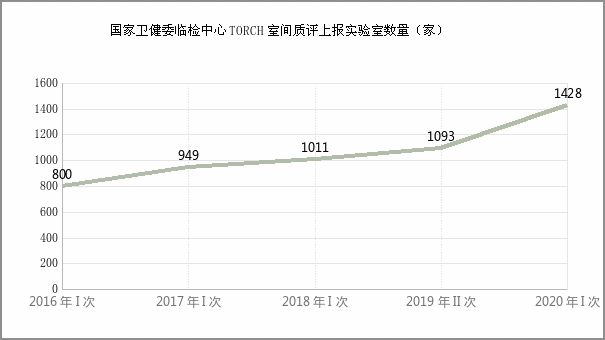
IgG和IgM抗体联合检测
是TORCH实验室规范化检测的基础
仅凭IgM抗体阳性检测结果诊断急性感染是TORCH检测亟待规范的重点之一。
IgM抗体是病原体感染后机体内出现最早的抗体,IgM抗体阳性提示患者可能处于急性感染期。TORCH的原发感染和复发感染均能产生IgM抗体,因此仅IgM抗体阳性检测结果不能诊断急性感染,也不能区分原发感染和复发感染。
五聚体结构的IgM易于与有重复决定簇的抗原结合,易出现交叉反应,可能出现假阳性结果。另外由于部分人群体内的IgM抗体可以保持较低的滴度水平,并可持续表达数年。IgM抗体假阳性与持续阳性两种情况则会给临床诊断带来困惑,单做IgM往往得出个体正在急性感染错误的结果。
这一问题可通过同时检测IgG而得到满意的纠正。同时检测外周血IgG和IgM抗体,有条件实验室应尽可能采用定量检测方法。必要时,间隔2~4周后复查,以动态监测IgG。不能确定感染类型者,应进行IgG抗体亲合力检查。共识指出联合、定量检测IgG和IgM抗体,并动态分析是TORCH实验室规范化检测的基础。
综合近5年卫健委临检中心室间质评TORCH-IgM/IgG上报实验室数量分析,IgG抗体与IgM抗体检测比例逐渐趋于1:1。
|
实验室数量(家)
|
CMV(IgM:IgG)
|
|
2016年I次
|
1.24:1
|
|
2016年II次
|
1.24:1
|
|
2017年I次
|
1.21:1
|
|
2017年II次
|
1.21:1
|
|
2018年I次
|
1.18:1
|
|
2018年II次
|
1.17:1
|
|
2019年II次
|
1.14:1
|
|
2020年I次
|
1.16:1
|
|
2020年II次
|
1.16:1
|
TORCH定量分析
有助于发现假阳性或假阴性结果
妊娠期发生TORCH初次感染或复发感染时,体内产生IgG或IgM是一个急剧变化的过程,只有通过定量分析浓度变才能检测到。对于那些孕前未做过基础免疫状况评估的孕妇,选择两个时间点(T1,T2)检测IgG或IgM浓度(C1,C2),计算单位时间内浓度变化梯度,能有效地发现机体受到病毒攻击而发生的特异性免疫反应,但目前还没有参考值,较常用的是C2/ C1 >4倍。通过定量分析可发现假阳性或假阴性结果,国内关于TORCH的共识或指南均建议采用定量技术检测TORCH IgG和IgM抗体。
近5年来国家卫健委临检中心室间质评各实验室上报数据中化学发光(定量)平台占比由2016年第I次的31.6%上升至2020年第二次的60.81%。
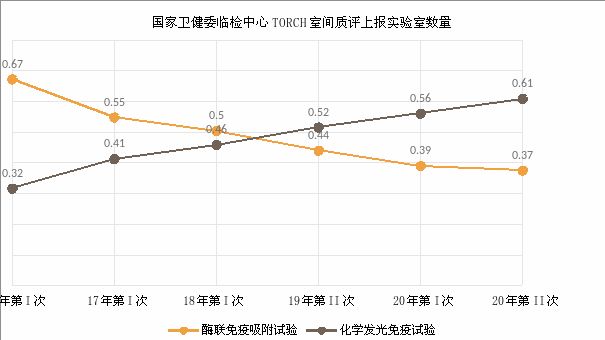
化学发光法检测TORCH抗体的批内、批间重复性好,灵敏度更高,对于TORCH感染的早期检测具有推广价值,在近年来TORCH抗体检测中受到了广泛关注。但考虑到不同区域检测平台的差异性,建议至少对IgG抗体进行定量检测,以动态观察抗体滴度变化。
单纯疱疹病毒是否分型检测
孕期单纯疱疹(HSV)感染以复发感染者多见,其经胎盘垂直传播导致胎儿感染的风险较小,而以阴道分娩时产道感染较多见。因此,对HSV感染孕妇应告知可能对胎儿产生宫内感染、产道感染的风险。建议在孕35~36周对此类孕妇定量检测血清IgM、IgG抗体。
单纯疱疹病毒分为1型和2型。研究表明 1型和2型疱疹病毒都能引起生殖器疱疹,2型相对多见。有观点认为由于HSV-1和HSV-2这两种病毒型在胎儿危害和临床治疗方法等方面没有区别,所以,围孕期进行HSV血清学筛查时不必分型检测。但是有研究发现复发生殖器疱疹常常和2型相关,1型生殖器疱疹复发频率远低于2型。鉴于二者感染率差别和感染特点差异,建议对 HSV IgG 抗体进行分型检测,以便提供一定的参考信息。
HSV是否分型检测的观点暂未统一,2020年国家卫健委临检中心TORCH室间质评上报实验室数据中HSV1-IgM、HSV2-IgM实验室家数均高于HSV1/2-IgM,且HSV1-IgG、HSV2-IgG上报实验室家数均高于HSV1/2-IgG,可见目前HSV分型检测仍是实验室使用的主流方法。
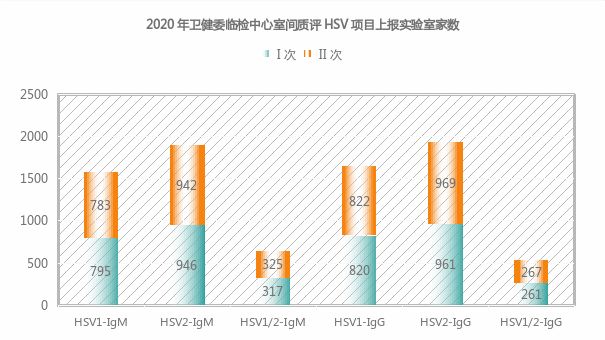
专家共识与“健康中国”
从“专家共识”看TORCH血清学检测可见:联合、定量检测IgG和IgM抗体是TORCH实验室规范化检测的基础,动态定量分析建议在同一检测体系上进行,同时应结合IgG抗体亲和力检测、TORCH病原体核酸分析等。临床实验室通过规范性检测获取的感染状态、感染类型、机体免疫状态等信息,可为临床诊治和评估妊娠风险提供可靠的依据。
随着检测技术的不断发展,急性感染期抗体水平升高的判断阈值、动态观察时间间隔等问题还需要在新的检测方法基础上验证和探索。进一步完善符合我国国情的实验室TORCH检测规范化流程还需要更多的循证医学依据。
TORCH实验室规范化检测与临床应用等相关TORCH共识、指南是深入贯彻“主动学习掌握出生缺陷防治知识”落实“健康中国2030”规划纲要》,是全面加强出生缺陷综合防治工作,预防和减少出生缺陷,提高出生人口素质、推进健康中国建设的重要举措。
参考文献
[1].朱宇宁,尚世强,陈英虎,陈大鹏,贾莉婷,渠巍,柯江维,李海波,李晓勤,梁秀云,刘艳秋,马丽娟,莫丽亚,阮强,沈国松,王雨新,许红,徐锦,徐两蒲,许晓红,袁恩武,张乐海,张文利,张欣文.TORCH实验室规范化检测与临床应用专家共识[J].中华检验医学杂志,2020,43(05):553-561.
[2].《“健康中国2030”规划纲要》[J].中国肿瘤,2019,28(10):724.
[3].章锦曼,阮强,张宁,李利,叶汉风,马艳萍,董旭东,孟昱时,朱宝生,李金明.TORCH感染筛查、诊断与干预原则和工作流程专家共识[J].中国实用妇科与产科杂志,2016,32(06):535-540.
[4].妊娠期ToRCH筛查指南[J].解放军医药杂志,2014,26(01):102-116.
[5].王谢桐,周乙华.妊娠期巨细胞病毒感染筛查与处理专家共识[J].中国综合临床,2018,34(01):1-4.
[6].DollardS C,StarasS A,AminM M,etal.Nationalprevalence estimates for cytomegalovirus IgM and IgG avidity andassociation between high IgM antibody titer and low IgG avidity[J].ClinVaccine Immunol,2011,18( 11) : 1895-1899.
[7].BenedettiJ, Corey L, Ashley R. Recurrence rates in genital herpes aftersymptomatic first‑episode infection[J]. Ann Intern Med, 1994,121(11): 847‑854. DOI: 10.7326 /0003‑4819‑121‑11‑199412010‑00004
[8].YinonY,FarineD,YudinM H,etal.Cytomegalovirusinfection in pregnancy[J].JObstet Gynaecol Can,2010,32( 4) : 348-354.
[9].SonoyamaA,EbinaY,MoriokaI,etal.LowIgG avidity and ultrasound fetal abnormality predict congenitalcytomegalovirus infection[J].JMed Virol,2012,84( 12 ) : 1928-1933.
[10].Nahmias AJ, Walls KW, Stewart JA, et al. The TORCH complex‑perinatalinfections associated with toxoplasma and rubella, cytomegol‑andherpes simplex viruses[J]. Pediatr Res, 1971, 5 (8): 405‑406.
DOI:https://doi. org / 10.1203/00006450‑197108000‑00144.
[11].di Carlo P,RomanoA,CasuccioA, et al. Investigation and man⁃ agement of Toxoplasma gondiiinfection in pregnancy and infan⁃cy: a prospective study[J]. ActaPharmacol Sin,2011,32(8):1063-1070.
编辑:Jason | 校对:Harris | 责编:Hillson
公司简介

德国维润赛润(Institut VirionSerion GmbH)成立于1978年,是国际知名的诊断产业原料生产商和供应商。公司的研发和生产基地位于德国维尔茨堡,已通过DIN EN ISO 13485质量体系认证,拥有三级生物安全实验室(P3实验室)。经过了40余年的发展,公司构建了丰富的生物原料产品线,主要包括天然抗原、重组抗原、人源化单克隆抗体和磁珠等。
产品信息
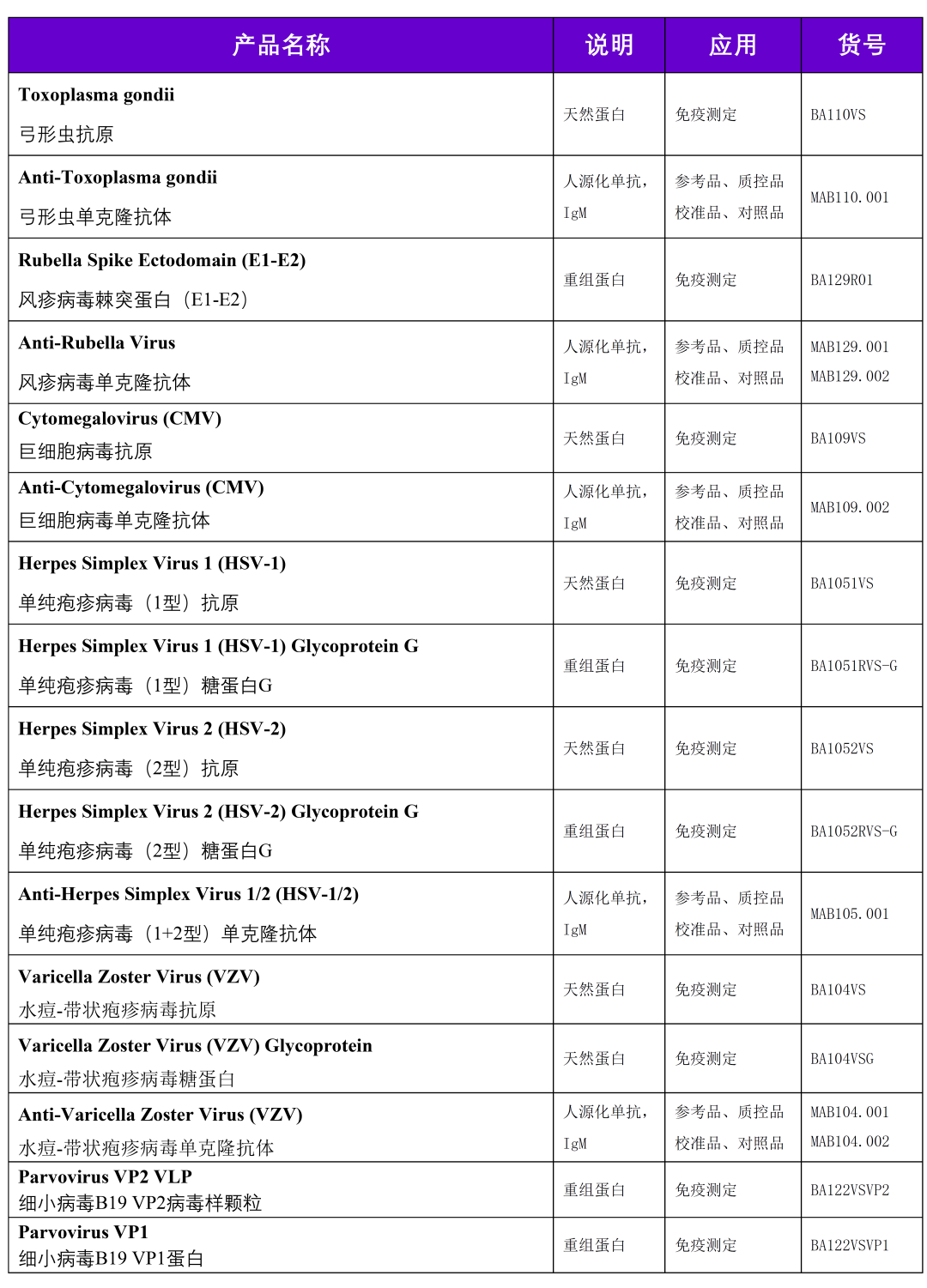
助力我们的客户更加强大
永葆我们的价值无可替代

免责声明:本微信号所发表文章出于传递和分享,不代表维润赛润资讯的观点和立场。如涉及版权等问题,请尽快联系我们,我们第一时间进行删除处理!若需转载,请加上贴片,欢迎联系小编开白。












