
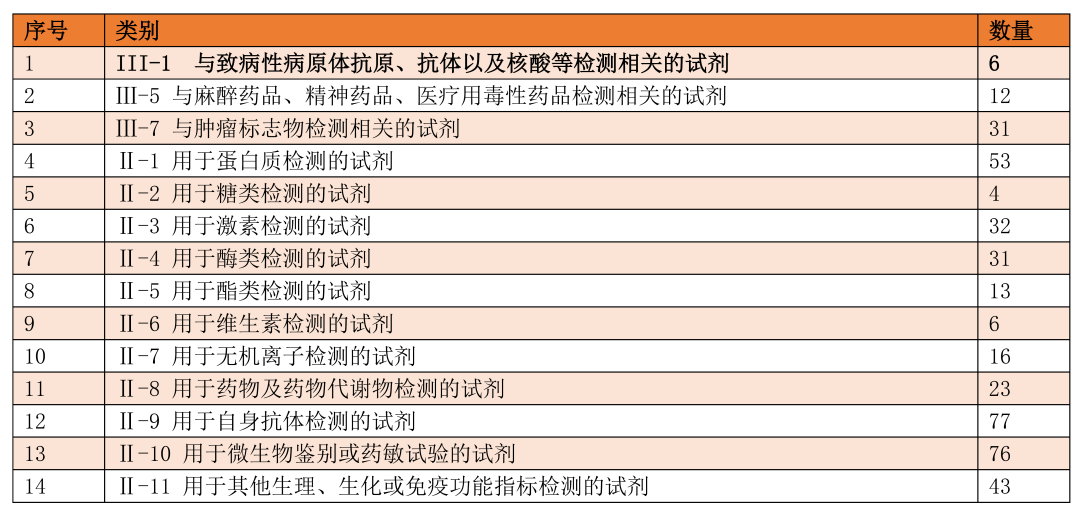
附件:免于临床试验体外诊断试剂目录
来源:国家药品监督管理局医疗器械技术审评中心 审评六部

公司简介



德国维润赛润(Institut Virion\Serion GmbH)成立于1978 年,是国际知名的诊断产业原料生产商和供应商。公司的研发和生产基地位于德国维尔茨堡,已通过DIN EN ISO 13485 质量体系认证,拥有三级生物安全实验室(P3 实验室)。公司基于不断的研发创新和为客户创造价值的理念,构建了丰富的免疫生物原料产品线, 主要包括天然抗原、重组抗原、人源化单抗、阻断剂和磁珠等。
维润赛润生物技术(深圳)有限公司是Institut Virion\Serion GmbH设立于中国的子公司。维润赛润(深圳)全面负责Virion\Serion产品在亚太地区的市场推广、商务合作、技术服务、应用研究。

|

|


附件:免于临床试验体外诊断试剂目录
来源:国家药品监督管理局医疗器械技术审评中心 审评六部

公司简介



