第十九届中国国际检验医学暨输血仪器试剂博览会(CACLP)
第二届中国国际IVD 上游原材料制造暨流通供应链博览会(CISCE)
CACLP展位号:B5-0805
展会时间:2022 年3 月27 日-3 月29 日
展会地点:南昌绿地国际博览中心
大家好,在上一篇文章当中,我们对免疫诊断试剂的验证方法和开发进行了初步的了解,今天我们将来了解一下在验证开始前,我们需要完成哪些工作。
一旦选择了最佳的抗体(或抗体组),并且确定了检测条件,包括校准曲线、检测限(LOD)、定量下限(LLOQ)、检测范围、重现性和稳定性等方面,就可以进行验证前研究研究。
实验室的实验记录是相当重要的存在,任何数据异常或方案偏差都应该被记录和解释。最好的做法是打出一份方案(按照标准操作程序执行),列出所有使用的材料,它们是如何组成的,以及方案的一步步细分,然后在这份清单上直接记录相应的实验结果。
在这个阶段,准备足够的试剂是很重要的,这些试剂将足以满足整个验证研究的需要。所有的校准样本(待测物样本)和抗体(最好是高度纯化的,以减少可能的检测干扰)都应该事先做好特征分析。
如果在验证过程中需要生产和纯化更多的待测物或抗体,就必须重新优化浓度和条件,这可能会影响测定的再现性。
这些试剂的储存应使重复使用不影响样本的完整性(即以等分的方式储存在-20℃或最好在-80℃)。
配体结合试验是依赖于待测物与生物分子的特定结合的方法。通常,这些都是受质量作用规律支配的可逆性结合事件。应进行适当的测定优化,以确保测定发挥其最大能力。例如,应根据经验评估最小稀释度、涂层浓度、结合物浓度、洗涤条件和孵化时间。
校准曲线的选择和制备是所有定量检测方法的设计、验证和应用的核心。从异质、不纯和/或特性差的待测物中制备的校准曲线更有可能产生更大的不确定性和更高的变异性。
选择的校准曲线应该是对你的数据给予最佳拟合的模型。
不理想的曲线拟合会增加检测的百分比误差,更有可能增加可以定义定量极限的浓度。配体结合试验(LBA)测量一系列遵循质量作用定律的相互作用的信号,从而形成非线性的、通常是正方形的标准曲线。
响应误差关系不是恒定的(异方差),因此,最高的精密度不一定与最高的灵敏度相一致。由于反应方差的这种异方差性质,四参数和五参数的逻辑校准曲线经常被用来拟合LBA标准曲线。
-
由于一旦开始检测验证,就不应该改变标准浓度,因此在方法开发和验证前研究期间应该包括更多的标准点和重复,以促进对浓度-反应关系的早期详细调查。
-
建议至少使用3次运行来建立校准曲线,其中至少有8个非锚定标准的重复运行。必须通过评估校准的反算浓度和标称浓度之间的相对偏差来验证模型的接受程度。不建议使用相关系数来确认回归模型。为了使一个模型能够被接受,建议在预期的验证范围内,校准器的平均%RE一般不超过10%。在某些情况下,如果偏差和精密度的差异实际上并不重要,那么选择一个更简单的模型比选择一个更准确但复杂的模型要好。一般来说,应该使用能够充分描述浓度反应的最简单模型。
-
如果不对不等的标准偏差进行适当的加权,曲线拟合会产生次优的结果,并对真正的检测性能进行不正确的评估(例如,灵敏度低和检测范围有限)。由于精确度随浓度的变化而变化,因此,如果曲线拟合程序对校准点进行加权,使更精确的校准点对曲线拟合的影响最大,那就更好。在大多数加权回归程序中,应用于每个点的权重是所用反应参数方差的倒数。这意味着方差越小,权重越大,从而迫使曲线拟合程序集中在校准曲线上具有最大精密度的那些点上。
解释免疫诊断试剂结果的一个挑战是了解该诊断试剂所检测的到底是什么。
这方面的基础是对抗体特异性(与相关化合物的交叉反应性分析)和灵敏度(在样本中存在其他蛋白质成分的情况下,检测方法只测量目标待测物的能力)的了解。
旨在确定抗体特异性的实验可以包括评估其与类似化合物的交叉反应性,在可行的情况下,建议在样本基质中加入生理化学上类似的化合物或目标待测物的变体。
在检测方式相对固定后,应在定量下限附近添加多批不同浓度的样本,并计算待测物的回收率。这将有助于最终选择一个定量下限,然后再开始进行检测验证。
了解灵敏度的另一个实验是在稀释剂和基质中加入标准曲线校准物,以检测校准范围内所有浓度的基质效应。
➤ 灵敏度
检测动态范围,也称为「可报告范围」,从定量下限(LLOQ)延伸到定量上限(ULOQ)。在这些范围内,被待测物可以在可接受的准确度、精确度和总误差水平上进行测量。
重要的是要理解LLOQ和ULOQ的选择,因为它们定义了标准曲线的真正的、可接受的极限。分别低于或高于LLOQ和ULOQ的标准曲线点被认为是外推的,不能用来报告样本的浓度。
LLOQ是在可接受的准确度和精确度下可以测量的标准曲线最低浓度。
在开发的早期,可以使用反算的标准值来产生定量范围的初步估计。之后,再使用加标样本来完善估计范围。
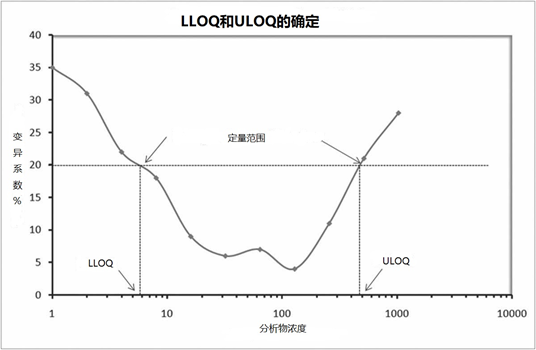
在这一阶段,在预期的低限值和超低限值区域包括更多的点是有用的。精确度曲线图(如图1所示)可以帮助评估预期的定量限。
图1|可用于计算定量下限和上限的典型精密度曲线的例子。由于测定间差异比测定内差异大,有必要从一段时间内的多次运行中获得精密度曲线的数据,而不是使用一组数据。
定量下限(LLOQ)是满足以下条件的最低标准:
方法精密度和准确度(如图2所示)是描述在特定条件下重复测量同一同质(加入标准样品)样本的随机误差(变异)和系统误差(平均偏差)大小的性能特征。
图2|准确度和精确度之间的关系示意图。准确度是指测试值与被待测物浓度的【真实】值之间的关系,而精密度是对重复测量结果的扩散的衡量,取决于随机误差的分布。
方法精密度和准确度应通过分析验证样本(QC样本)来评估,这些样本是在与预期研究样本相同的生物基质中制备的。
在验证前研究和临床前验证期间,要在多个检测批次中进行测量,并在每个批次中进行重复测定。
根据ICH指南,精密度又分为短期(运行内精密度或批内)和中间精密度(运行间或批间),测量精密度随时间变化,并可能涉及不同的分析人员、设备和试剂。
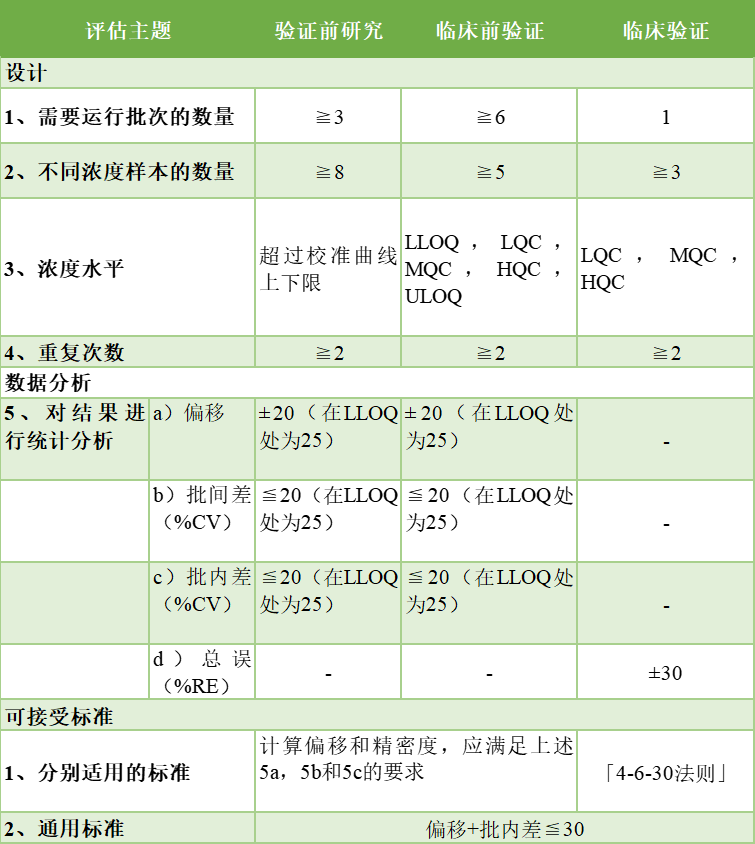
方法精密度、批内(运行内)精密度和批间(运行间)精密度应在验证前研究期间初步确定,并在临床前验证中确认。表1总结了对精密度和准确度评估的设计和分析建议。
表1 | 精密度和准确性评估标准。推荐的分析和验收标准适用于分析的每个样本浓度。
-
进行3个批次的运行(3个独立的检测),至少有8个样本(越多越好),对于批次间的研究是一式两份(或三份),对于批次内的研究是5~6次重复。
-
通过计算变异系数来分析重复结果的精确度(批内重复≥5次,批间重复≥2次)。
-
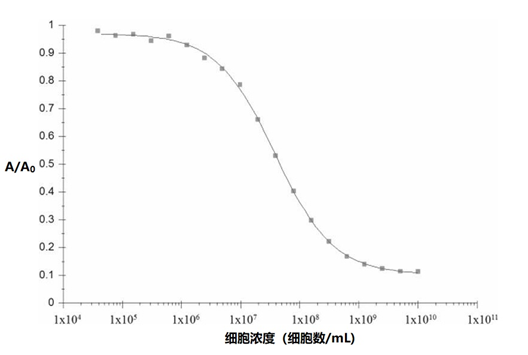
将最佳校准曲线应用于平均数据,并通过反向计算已知标准的预测浓度来确定检测的准确度(如表2和图3所示)。
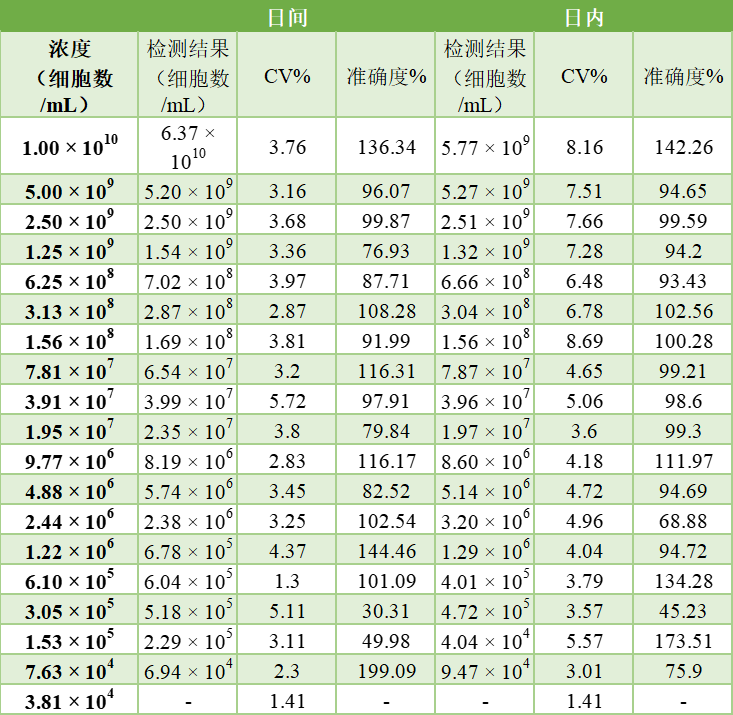
表2 | 抗单核细胞增生李斯特菌抗体的日间检测校准曲线。
对数据集进行了4参数方程的拟合。含有破折号的单元格表示由于数据点不符合校准曲线,所以无法获得任何数值方差系数(精密度的定量测量)用公式%CV=(SD/Mean)×100计算,其中对于日内研究,标准偏差(SD)是从一次验证运行中的重复(5次重复)分析中计算出来的,对于中间精密度(日间),SD是从5天内的重复(3次重复)分析中计算出来的。
图3|从李斯特菌单核细胞增生的免疫测定中计算出的测定准确性和精确度的例子。曲线上的每个点是五天内五个重复测量的平均值, A/A0是归一化的吸光度,其中A0代表没有细胞存在时的数值。
空白限(LOB)、检测限(LOD)和定量下限(LLOQ)这些术语描述了一个诊断试剂可以可靠地测量的最小的分子浓度。
为了建立这些参数,研发人员应该测试大量的样本重复,以提高估计值的稳定性和统计学上的可信度。
LOB和LOD对于区分待测物的存在与否的测试很重要,而LLOQ对于可靠地测量低水平的待测物是必要的(即LOD=定性数据,LLOQ=定性和定量数据)。
从本质上讲,检测限是指测量值大于与其相关的不确定性的点。它是样本中能被检测到的最低待测物浓度,但不一定能被量化。
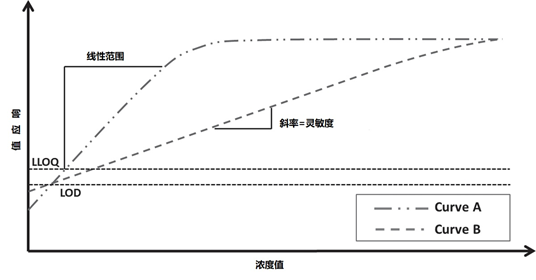
LOD经常与分析方法的灵敏度相混淆。一个分析方法的灵敏度是指该方法对测试待测物的浓度或质量的微小差异进行区分的能力。在实际应用中,灵敏度是指通过绘制反应与被待测物浓度的关系而得到的校准曲线的斜率(如图4所示)。
图4|展示检测灵敏度和检测限的实例图。曲线A和B都有相同的LOD,但对待测物浓度的差异有非常不同的敏感度。曲线A的线性范围比曲线B窄,但在这个范围内的灵敏度要高得多。
LOD是一个公认的参数,用于描述分析确认方法的特点。它可以被定义为可能从空白限(LOB)中可靠地区分出来的最低待测物浓度,并且在该浓度下检测是可行的,因此,它大于LOB。
一个典型的估计LOD的方法包括测量一个零校准物或空白样本的重复,通常是n=20,确定平均值和SD,并将LOD计算为平均值+2SD。
这种方法的变种是用平均值加3、4、甚至10个SD来提供一个更保守的LOD。
这是一个简单而快速的方法,但缺点是没有客观证据证明低浓度的待测物确实会产生可与空白(零浓度)样本区分的信号。
另一种方法是利用对含有少量但已知浓度的有关物质的样本进行分析。这种经验性方法的优点是利用客观数据来比较空白和低浓度样本的分析反应,以最终确定什么浓度的待测物是区分其存在和不存在的必要条件。
建议免疫诊断试剂的生产厂商用于建立这些参数的LOB和LOD样本的实际数量为60个,而在实验室验证制造商的LOD(可能还有LOB)时,样本数量为20个。
一旦确定了临时的LOD,就可以通过检查含有LOD浓度的样本的观察值来确认它。
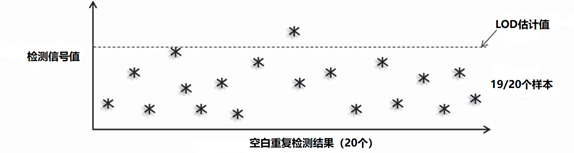
一些LOD样本值预计会小于估计的LOD(如图5所示),但是采用参数方法,用平均值加上1.645×SD,其中1.645是正态分布的第95个百分位数,不超过5%的值应该小于LOB。
图5|实验确定检测的LOD的例子
如果观察到的LOD样本值符合这个标准,那么LOD就被认为是成立的或被验证的。如果超过5%(大约20个观察值中的1个)的LOD样本值低于LOB,则LOD太低,必须重新估计(即通过测试一个更高浓度的样本,产生更高的平均值和SD,从而产生更高的LOD)。
实验中需注意的要点:
✔ 分析(20~60个)空白样本,用LOB=平均空白+1.645×(SD空白)来确定空白的极限。
✔ 分析(20~60个重复)处于和高于LOB的样本,以验证它们与空白19/20倍的区别。
✔ 用LOD=LOB+1.645×(SD低浓度样本)计算出可与空白区分的最低待测物浓度19/20倍的LOD。
如果有的话,应购买或寻找参考测定法或公认比较稳定的诊断试剂,以便将正在准备的测定法与以前验证的方法进行比较。
这为新的检测方法的验证增加了可信度,并使人们能够直接比较任何检测方法的改进。这也有助于证明抗体的灵敏度,因为回收(或检测)的待测物可以用标准方法进行验证。
在进行研究前的验证实验之前,应准备好所有的试剂并记录在案,准备一份打印好的详细SOP,并记录任何与之相背离的原因。
理想的情况下,验证样本应该是加标的真实样本(例如,加标待测物的阴性患者血液「10~20个供体」或从已知药物浓度的组织源中提取的药物)。
在验证前研究和临床前验证之间的关口,人们有可能区分标准曲线和校准曲线(尽管这些术语通常是同义的)。
到目前为止,标准曲线是由大量的标准品组成的,所有这些标准品都有助于定义曲线拟合、LOD和LLOQ。
在研究前的验证中,需要较小范围的样本(经过良好的校准,即校准样本),这些样本要跨越测定的范围。
因此,校准曲线将使用标准曲线确定的曲线拟合来拟合少量的校准样本。校准样本应包括低、中、高浓度的样本和处于LOD和LLOQ的样本。还应包括一个空白样本。
如何从组织中提取待测物(如从肉中提取的药物)或如何提取和储存血样都会影响测定的敏感性和准确度。
低效率的提取会降低检测的整体功能灵敏度,例如,所开发的检测方法可能能够定量到1 ng/mL,但如果提取过程只有10%的效率,那么实际的检测灵敏度是10 ng/mL,因为90%的样本被丢失。
血液样本通常是在带有抗凝血剂的试管中提取和储存的,这可能会影响检测结果。此外,正在接受心血管疾病治疗的病人可能正在接受肝素或华法林治疗,这可能会影响测定法准确检测待测物的能力。
应该对这些因素进行调查,因为它们会影响测定的稳定性。当这种操作可能会影响到样本和/或待测物的完整性时,及早、一致地应用预定的样本采集和处理技术尤为重要。
-
选择合适的样本,并将其分为两份,其中一份样本中加入待测物标准品。
-
使用验证前研究中的优化检测条件和校准标准来分析提取的普通样本和加标样本。
-
计算提取效率为((加标样本的浓度-普通样本的浓度)/加入标准品的浓度)×100。
对于研究含有不同内源性干扰血液样本实验中需注意的要点:
-
使用因子法(即分别和组合添加EDTA、肝素和华法林,再加上没有污染物的阴性血样),同时也准备具有待测物和可能污染物的阳性血样。
-
将待测物(通常是一种蛋白质)加入到上述准备好的血样中。
-
使用验证前研究中的优化的分析条件和校准标准来分析血样和加标的样本。
-
对于阴性样本,计算检测效率为(阴性血样中的待测物检测浓度/加入待测物的浓度)×100
-
对于阳性样本,计算检测效率为((阳性血样中的待测物检测浓度-阳性血样中待测物原浓度)/加入待测物的浓度)×100。
好了,以上就是今天分享的全部内容,如果大家有什么疑问,欢迎在后台给我们留言,或者加入我们一起讨论~

编辑:Jason | 校对:Harris | 责编:Hillson
公司简介

德国维润赛润(Institut VirionSerion GmbH)成立于1978年,是国际知名的诊断产业原料生产商和供应商。公司的研发和生产基地位于德国维尔茨堡,已通过DIN EN ISO 13485质量体系认证,拥有三级生物安全实验室(P3实验室)。经过了40余年的发展,公司构建了丰富的生物原料产品线,主要包括天然抗原、重组抗原、人源化单克隆抗体和磁珠等。
产品信息
产品咨询
SERION原料事业部:
18818686988 0755-89381139

助力我们的客户更加强大
永葆我们的价值无可替代

免责声明:本文仅代表作者本人观点,不代表维润赛润资讯的观点和立场。文章图片均来源于网络,如有侵权,请联系作者删除,欢迎联系小编。